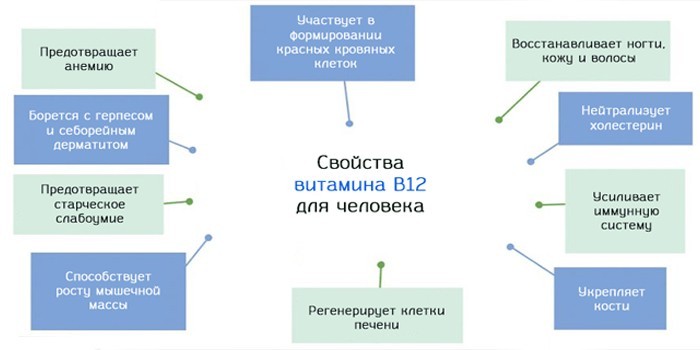
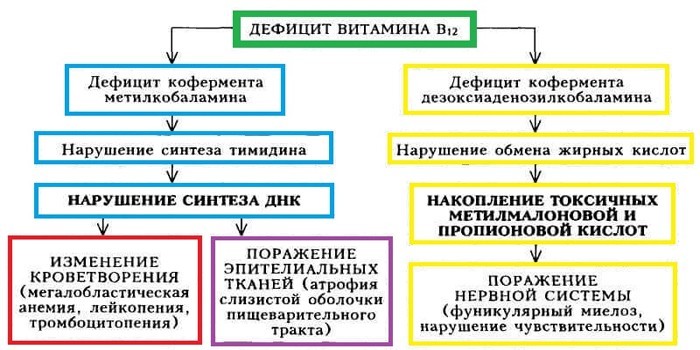
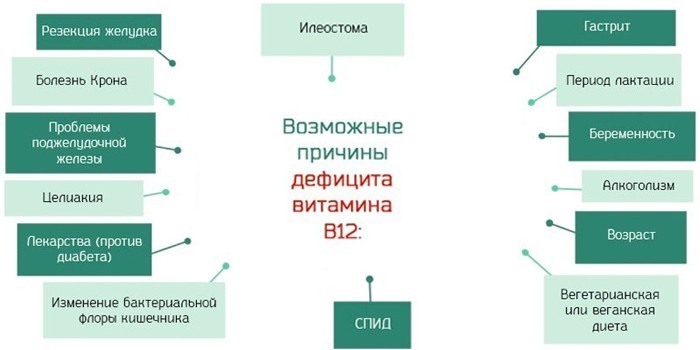
Витамин B12, или цианокобаламин, поступает в организм с пищей. Содержится в продуктах животного происхождения: мясе, молоке, яйцах. Витамин B12 необходим для выработки красных клеток крови. При его недостатке возникает малокровие.
В медицине авитаминоз В12 называют мегалобластной анемией. Если болезнь вовремя выявлена, а назначенное лечение дает результаты, бояться нечего. Хуже, когда анемия запущенная и плохо поддается терапии.
Суточная норма цианокобаламина у мужчин и женщин составляет 2,6 мкг. Беременным, кормящим нужно 2,8 мкг витамина ежедневно. Недостаток цианокобаламина развивается постепенно. На начальных этапах проявляется слабостью, тошнотой. Со временем признаки дефицита витамина В12 нарастают:
- кожа бледнеет;
- немеют руки, ноги;
- ухудшается внимание;
- воспаляется язык;
- появляется одышка;
- болит живот;
- кружится голова;
- ухудшается зрение;
- возникает депрессия.
Нехватка витамина В12 влияет на интимную сферу. Сказывается на качестве спермы, половой жизни, вызывает:
- нарушение координации;
- головные боли;
- уменьшение объема мышц;
- покалывание в руках, ногах;
- сильную депрессию;
- усталость.
На начальных этапах дефицит витамина B12 проявляется перепадами настроения. Со временем у женщин:
- нарушается менструальный цикл;
- учащается пульс;
- выпадают волосы;
- ухудшается память;
- немеют конечности.
До года ребенку требуется не менее 0,4 мкг витамина в день. С года до пяти лет суточная норма увеличивается до 1 мкг. Ребятам постарше нужно до 2 мкг витамина ежедневно. При нехватке В12 у детей наблюдаются:
- снижение интеллекта;
- плохая память;
- неуклюжесть;
- плохое зрение;
- слабость;
- бледная кожа;
- головные боли;
- снижение аппетита;
- неспособность к обучению.
Признаки дефицита цианокобаламина у грудничков:
- плохой аппетит;
- недобор веса;
- язвы во рту;
- вздутие живота;
- запоры;
- одышка.
Недостаток витамина В12 у детей проявляется:
- слабостью;
- мышечной болью;
- головокружением;
- запором.
Нехватка цианокобаламина замедляет развитие мозга у маленьких детей. Таким ребятам сложнее:
- распознавать буквы;
- научиться говорить;
- оценивать чувства других детей;
- собирать пазлы;
- решать простые задачи.
Дефицит витамина B12 развивается по двум причинам:
- Недополучение с пищей – происходит при нарушении питания, алкоголизме.
- Плохая всасываемость в кишечнике – вызвана болезнями желудка, тонкой кишки и гельминтами.
В группе риска развития дефицита цианокобаламина:
- пожилые;
- вегетарианцы;
- пациенты после операции на тонкой кишке;
- диабетики;
- больные с синдромом Крона.
Среди осложнений авитаминоза B12:
- поражение спинного мозга;
- хронические болезни печени;
- детский церебральный паралич;
- умственная отсталость;
- кожные болезни;
- бесплодие;
- слепота;
- онкология.
Начинают с коррекции питания. Потребляют больше белковой пищи.
При нарушении кислотности желудка, функции всасывания принимают витаминные комплексы.
источник
В12-дефицитная анемия является заболеванием, суть которого состоит в нарушении кроветворения, связанном с дефицитом в организме ребенка витамина В12 (цианокобаламина). Она относится к разновидности мегалобластных анемий. Ее называют еще пернициозной, то есть в переводе с латинского языка опасной.
Этот витамин в организм попадает из пищевых продуктов. Цианокобаламин, или витамин В12, связывается в желудке с выработанным слизистой глюкопротеином и другими R-протеинами (белками), входящими в состав слюны и желудочного сока. Эти связующие факторы защищают витамин от разрушения в пищеварительном тракте.
В тонком кишечнике ферменты поджелудочной железы способствуют отсоединению цианокобаламина от транспортных R-протеинов и соединению с внутренним фактором. В подвздошной кишке этот комплекс соединяется с эпителиальными клетками слизистой.
Освобождение витамина от фактора Кастла и эпителия осуществляется с помощью специальных белков сыворотки крови (транскобаламинов), доставляющих цианокобаламин к тканям.
С кровью витамин заносится:
- в костный мозг, где его участие необходимо в выработке эритроцитов;
- в печень для создания его запаса;
- в ЦНС, где он участвует в синтезе миелиновой оболочки вокруг нервных волокон.
Запас цианокобаламина в организме составляет примерно 5 мг, а суточные потери его равны 5 мкг.
Слева — нормальные клетки крови, справа — таковые при мегалобластной анемии.
Наиболее чувствительны к недостатку витамина В12 нервная система и красный костный мозг. В первую очередь страдает кроветворение. Образование эритроцитов становится неэффективным – появляются вместо нормальных клеток мегалобласты.
Часть из них уничтожается организмом сразу же, продолжительность жизни остальных тоже меньше, чем у нормальных эритроцитов. В связи с этим в крови число красных кровяных клеток значительно снижается – возникает анемия. Усиленное разрушение (гемолиз) несостоятельных клеток приводит к увеличению селезенки, повышенному уровню билирубина в крови и уробилина в моче.
Снижение числа тромбоцитов в крови повышает риск возникновения кровотечений. А сниженное содержание лейкоцитов в кровотоке создает угрозу развития инфекций.
Недостаточное обеспечение тканей кислородом приводит к развитию дистрофических изменений в сердечной мышце, печени и других органах, атрофии слизистой пищеварительного тракта. В нервных волокнах разрушается миелиновая оболочка, что приводит к нарушению проведения нервных импульсов.
Дефицит витамина В12 может вызвать также недостаточное содержание в организме фолиевой кислоты. Без этих двух компонентов невозможен процесс синтеза ДНК в клетках. Поражением нервной системы отличается В12-дефицитная анемия от мегалобластной фолиеводефицитной. Но так как цианокобаламин и фолаты тесно связаны друг с другом, нередко возникает в организме двойной дефицит – недостаток этих двух веществ одновременно.
Причин возникновения пернициозной анемии достаточно много:
- Недостаточное содержание витамина в продуктах рациона:
- несбалансированное питание ребенка;
- вегетарианство (многие родители с раннего детства приучают детей к такой системе питания, исключающей в зависимости от вида вегетарианства употребление мяса, молока, яиц и т. д.);
- у грудничка дефицит может создаваться при грудном кормлении матерью-вегетарианкой.
- Нарушение усвоения и всасывания витамина:
- недостаточное выделение фактора Кастла в результате:
а) врожденного дефекта слизистой желудка или структуры самого фактора;
б) воспаления слизистой при гастрите;
в) вследствие разрушения клеток, выделяющих внутренний фактор, аутоантителами;
- снижение секреции поджелудочной железы, что приводит к нарушению расщепления белка R, необходимого для связи витамина В12 с гастромукопротеидом;
- изменения в тонком кишечнике, снижающие всасывание:
а) воспалительный процесс (при хроническом энтероколите);
б) удаление части кишечника оперативным путем;
в) дисбиоз микрофлоры кишечника;
г) злокачественные новообразования;
д) глютеновая энтеропатия (целиакия);
ж) дивертикулит тощей кишки (нарушение структуры, выпячивание стенки кишки).
- Повышенные потребности в витамине В12:
- при повышенной выработке гормонов щитовидной железой;
- в периоды интенсивного роста организма;
- при уменьшении числа эритроцитов вследствие повышенного разрушения их;
- при поглощении витамина бактериями или гельминтами (особенно при инвазии лентецом широким).
- Неполноценное использование витамина В12 в организме:
- отсутствие депо витамина при патологии печени.
- Увеличение потерь витамина:
- повышенное его выделение из организма за счет недостаточной связи с белком при некоторых врожденных патологиях;
- при гемодиализе.
- Длительное лечение такими лекарственными препаратами, как:
- Фторурацил;
- Азатиоприн;
- Метотрексат;
- 6-Меркаптопурин;
- Цитозар;
- Сульфасалазин;
- Колхицин;
- Ацикловир;
- Триамтерен;
- Фенобарбитал;
- Неомицин и др.
Анемия по степени тяжести может быть легкой, среднетяжелой и тяжелой. Все клинические проявления пернициозной анемии у детей можно объединить в 3 группы: поражение системы кроветворения проявляется анемическим синдромом, пищеварительной системы – гастроэнтеритическим или диспепсическим синдромом, ЦНС и периферических нервных волокон – неврологической симптоматикой.
Клиника анемии развивается исподволь, симптомы появляются и нарастают малозаметно.
Для анемического синдрома характерны:
- слабость;
- головокружение;
- бледные кожные покровы имеют желтушный оттенок;
- возможна легкая желтушность склер;
- бледность видимых слизистых;
- мелькание черных точек перед глазами;
- шум в ушах;
- извращение вкуса (дети могут есть землю, мел).
Возникающая гипоксия тканей приводит к ухудшению состояния кожи (она становится сухой, шершавой), волос (они теряют блеск и секутся), ногтей (появляется расслоение, ломкость и исчерченность их).
В связи со снижением количества тромбоцитов характерны частые носовые кровотечения. При незначительной нагрузке дети быстро устают, отмечается одышка и увеличение частоты сокращений сердца. При далеко зашедшей анемии появляются выраженные отеки.
Поражение ЖКТ, или диспепсический синдром, проявляется:
- отсутствием аппетита (иногда даже отвращением к пище);
- явлениями глоссита (воспаления языка): язык со сглаженными сосочками приобретает яркий розовый цвет («лакированный» язык), беспокоят боли и жжение языка;
- нарушением стула в виде поносов и запоров;
- тошнотой и рвотой;
- вздутием живота из-за ухудшения переваривания пищи за счет снижения секреторной функции пищеварительных органов;
- увеличением размеров селезенки и печени;
- тяжестью или болями в животе;
- снижением веса тела.
Эти проявления не являются специфическими, они отмечаются при всех видах анемий. В отличие от них при В12-дефицитной анемии характерными являются проявления фуникулярного миелоза (за счет потери миелиновой оболочки нервов и нарушения передачи нервных импульсов к органам):
- нарушение координации и походки;
- скованность движений;
- мышечная слабость;
- межреберная невралгия (боли по ходу межреберий);
- ощущение покалывания в кистях и стопах;
- может быть энурез (недержание мочи).
Гипоксия головного мозга клинически выражается обмороками, расстройствам интеллекта, ухудшением памяти, невозможностью сосредоточиться. В результате этого страдает успеваемость у школьников. Могут поражаться слуховой, зрительный, обонятельный нервы, что проявляется нарушением обоняния, слуха, зрения и цветоощущения. Дети становятся эмоционально лабильными, легко раздражаются.
При длительно нелеченной пернициозной анемии возможно развитие комы, связанной с тяжелой ишемией вследствие гипоксии головного мозга.
Заподозрить анемию у ребенка врач может на основании жалоб (самого маленького пациента или родителей) и осмотра, а подтвердить диагноз «анемия» и определить ее вид помогут лабораторные методы исследования. Правильная диагностика очень важна, так как только она позволяет назначить адекватное лечение.
В12-дефицитная анемия характеризуется такими изменениями при лабораторных исследованиях:
В анализе крови (клиническом):
- сниженное количество эритроцитов;
- низкий уровень гемоглобина;
- повышенный цветной показатель;
- макроцитоз (клетки крови больших размеров);
- наличие в эритроцитах телец Жолли и колец Кебота;
- наличие мегалобластов (несозревших эритроцитов);
- снижение уровня тромбоцитов (кровяных пластинок);
- понижение числа лейкоцитов;
- повышение количества гиперсегментированных лейкоцитов;
- снижение ретикулоцитов (молодых эритроцитов).
Типичным для любой анемии является анизоцитоз (наличие наряду с нормальными эритроцитами клеток чрезмерно больших размеров и уменьшенных клеток – микроцитов; а также пойкилоцитоз: эритроциты с измененной формой (овальной, грушевидной вместо круглой).
При В12-дефицитной анемии отличительной характеристикой является гиперхромия (интенсивная окраска эритроцитов за счет повышенного содержания в них гемоглобина).
Учитывая то, что изменения в периферической крови не являются специфичными и встречаются при других видах анемий или при лейкозе, обязательно проводится стернальная пункция и исследование костного мозга.
Миелограмма (анализ полученного пунктата костного мозга) характеризуется мегалобластическим типом кроветворения:
- количество эритроидных клеток повышено в 2-3 раза;
- наличие мегалобластов с характерной ядерно-цитоплазматической диссоциацией: зрелая цитоплазма и нежная сетчатая структура ядра с необычно расположенным хроматином в виде ядрышек.
Биохимический метод исследования крови применяется для оценки состояния внутренних органов. Результаты могут помочь в установлении причины болезни, и они учитываются при подборе оптимального лечения.
При данном виде анемии может повышаться содержание билирубина в крови (преимущественно непрямой его фракции), железа, ферритина. Активность фермента ЛДГ (лактатдегидрогеназы) высокая и растет при прогрессировании болезни.
Содержание цианокобаламина в сыворотке крови низкое, хотя может быть нормальным (в зависимости от механизма развития анемии).
Для определения причины развившейся анемии могут использоваться аппаратные диагностические исследования: УЗИ, ФГДС, колоноскопия, МРТ.
Лечение назначается в зависимости от тяжести анемии, возраста ребенка, наличия неврологической патологии.
Принципы лечения анемии у детей:
- выявление и устранение (при возможности) причины анемии;
- насыщение организма цианокобаламином;
- поддерживающее лечение;
- диетотерапия.
При выявлении патологии ЖКТ назначается соответствующая терапия, включая ферментативные препараты (Креон, Фестал, Панзинорм) для устранения бродильной и гнилостной диспепсии. При глистной инвазии проводится дегельминтизация. Нормализовать состав микрофлоры в кишечнике помогут эубиотики (Бифидумбактерин, Бифиформ, Линекс, Лактобактерин и др.).
В комплексное лечение входит введение в инъекциях цианокобаламина. Дозы препарата и длительность курса определяет врач. После основного курса проводится поддерживающая терапия. Дети с В12-дефицитной анемией нуждаются в диспансерном наблюдении педиатра или гематолога. Им необходим мониторинг показателей периферической крови, при необходимости назначаются повторные курсы лечения.
Переливание крови (эритроцитарной массы) показано только в критических ситуациях при показателях гемоглобина менее 70 г/л и угрозе для жизни ребенка.
При одновременном дефиците фолиевой кислоты назначается введение ее в виде медикаментозных препаратов, а также учитывается этот факт при составлении рациона. При выявлении аутоантител к гастромукопротеину детским гематологом назначаются кортикостероидные препараты.
Длительный курс цианокобаламина может привести к снижению уровня калия в организме. Именно поэтому этот показатель должен периодически контролироваться и при необходимости корректироваться назначением препаратов калия.
При наличии неврологической симптоматики дополнительно назначаются другие витамины группы В (В1, В6).
Непременно в комплекс лечения входит сбалансированное питание, способное обеспечить организм ребенка в достаточном количестве не только витаминами, а и белками. Пополнить запас витамина В12 помогут богатые им продукты. Нормы потребления цианокобаламина зависят от возраста ребенка.
Суточная потребность детей в витамине В1:
| Возраст ребенка | Потребность в мкг |
| До 6 мес. | 0,4 |
| До 1 года | 0,5 |
| С 1 до 3 лет | 1,0 |
| С 3 до 6 лет | 1,5 |
| С 6 до 10 лет | 2,0 |
| Подростки | До 3,0 |
Рекомендуется вводить в рацион детей продукты, богатые витамином В12.
Содержание витамина В12 (в мкг) в 100 г продуктов:
- Печень (говяжья – 60; куриная – 16,6; свиная – 30).
- Мясо (свинина – 2; говядина – 2,6; крольчатина – 4,3; баранина – 2; сердце (субпродукт) – 25).
- Рыба (скумбрия – 12; карп – 1,5; сардина – 11; треска – 1,6).
- Осьминог – 20.
- Творог – 1,0.
- Брынза – 1,0.
- Сыр (Голландский – 1,4; Российский – 1,5).
- Бифидолакт – 1,4.
- Ацидофилин – 0,33.
- Кефир – 0,34.
- Сметана – 0,36.
- Сливочное масло – 0,07.
- Молоко – 0,4.
- Куриное яйцо – 0,52.
Проводимое лечение улучшает состояние и самочувствие ребенка. Спустя 12 ч. после инъекции цианокобаламина кроветворение в костном мозгу становится нормобластным.
Повышение ретикулоцитов отмечается с 3 дня лечения, а с 4 по 10 день возможен ретикулярный криз (значительное их повышение). Если ретикулез не появляется, значит, диагноз неправильный. Гиперсегментация лейкоцитов держится до 2 недель.
Все показатели крови приходят в норму спустя 1-2 месяца. Неврологическая симптоматика исчезает через полгода.
О профилактике анемии у ребенка следует позаботиться еще до рождения малютки. Беременная женщина должна, во-первых, правильно питаться и придерживаться всех рекомендаций по режиму, во-вторых, регулярно контролировать анализ крови. При развитии анемии у беременной женщины значительно возрастает риск ее возникновения у грудничка.
После рождения оптимальное питание для крохи – материнское молоко. В период лактации кормящей матери тоже очень важно обеспечить правильное питание. С 6-месячного возраста следует вводить малышу прикорм, соблюдая при этом все рекомендации педиатра. В 6 и в 12 месяцев ребенку проводят анализ крови.
Более старшие дети должны находиться под наблюдением педиатра и ежегодно сдавать анализ крови. Питание детей должно быть сбалансированным, обеспечивать ребенка всеми необходимыми растущему организму питательными веществами и витаминами. Важно своевременно выявлять и лечить гельминтозы, воспалительные заболевания ЖКТ, которые могут вызывать анемии.
Причины развития мегалобластной В12-дефицитной анемии разнообразны. Некоторые из них являются проявлением наследственной патологии, но многие можно предупредить, позаботившись об этом еще до рождения малыша.
Рациональное питание будущей матери и детей на протяжении всей жизни, регулярное врачебное наблюдение – вот те азы, которые помогут вырастить ребенка здоровым.
Важным моментом является своевременное диагностирование и лечение развившейся В12 –дефицитной анемии, не допускающее развития серьезных неврологических и дистрофических нарушений.
источник
В химическом отношении витамин В12 относится к группе кобаламинов. Он содержится в тканях животных, но отсутствует в растениях. Витамин в тканях животных является производным бактерий, которые представляют собой единственные организмы, способные синтезировать витамин В12 в природе. В тканях животных особенно богатым источником активности В12 является печень. В основном эта активность представлена коферментом, связанным с 5-дезоксиаденозином и со специфическим белком. Замещение дезоксиаденозилового радикала гидроксильными, цианидными или метальными группами ведет к образованию гидроксициано- или метилкобаламинов. Эти производные присутствуют в неболыпх количествах в тканях и плазме. Вероятно, они являются промежуточными метаболитами В12. В лечебных целях применяются гидрокси- и цианокобаламины. Введенный парентерально цианокобаламин in vivo быстро превращается в другие формы.
Главные из известных биохимических реакций в метаболизме млекопитающих, в которых участвует В12, — это:
а) перенос метиловой группы от 5-метилтетрагидрофолата гомоцистеину с образованием метионина;
б) внутримолекулярная перестройка атомов углерода в метилмалонил кофермента А с образованием сукцинил кофермента А.
Связь этих метаболических реакций, зависимых от B12, с развитием мегалобластиых изменений при дефиците В12 неясна. Гипотеза «ловушки» фолата уже не может объяснить все наблюдающиеся факты. У детей описаны редкие наследственные нарушения с дефектом обеих названных выше зависимых от кофермента В12 реакций, вследствие чего чрезмерно увеличивается экскреция метилмалоновой кислоты и гомоцистеина, однако, несмотря на наличие этих метаболических блоков, эритропоэз остается нормальным. У некоторых же больных наблюдаются неврологические нарушения с умственной отсталостью, усиленными сухожильными рефлексами и нарушенной проприоцепцией. Чанарин предполагал, что гемопоэтические эффекты дефицита B12 имеют совершенно иной механизм, отличающийся от механизма, воздействующего на нервную ткань, и от биохимических реакций. На основании изучения поглощения фолата лимфоцитами и костномозговыми клетками было высказано предположение, что дефицит В12 нарушает транспорт 5-меметилтетрагидрофолата в клетки крови, что ведет к мегалобластный изменениям.
Можно выделить три стадий всасывания. Вначале происходит взаимодействие пищевого витамина В12 с желудочным внутренним фактором (ВФ) с образованием макромолекулярного комплекса ВФ-В12. Затем этот комплекс связывается со специфическими поверхностями рецепторов на клетках слизистой подвздошной кишки. На третьем этапе включается механизм активного транспорта через кишечные клетки.
Во время транспорта в портальной крови В12, как предполагается, связывается с транскобаламином II (ТК-II), а не с ВФ. ТК-II имеет электрофоретическую подвижность бета-глобулина, в циркулирующей крови в основном не насыщен и легко связывает витамин В12 при введении его внутрь, или парентерально. Витамин В12, связанный с ТК-II, имеет короткий полупериод жизни, и ТК-II усиливает поглощение В12 рядом человеческих клеток, включая эритроциты. Другой белок, связывающий В12, TK-I с электрофоретической подвижностью альфа-глобулинов, почти полностью насыщен, имеет полупериод жизни 9-10 дней и нелегко обменивается с тканями. В свете этих данных можно предполагать, что главным транспортным белком для В12 служит ТК-II, а TK-I образует циркулирующий комплекс для депонирования В12. Клинический вывод: врожденный дефицит ТК-II вызывает мегалобластную анемию и системные проявления в первые несколько недель жизни при нормальном уровне В12 в сыворотке, а врожденный дефицит TK-I ведет к низкому уровню B12 в сыворотке без существенных проявлений дефицита.
Ключевым методом определения уровня В12 в сыворотке является микробиологическая проба. Нормальное содержание у взрослых составляет от 140 до 900 пг/мл, причем величины между 100 и 140 считаются пограничными.
Дорманди и соавторы также обнаружили колебания уровня от 220 до 770 пг/мл у 12 детей в возрасте моложе 1 года и от 150 до 1180 пг/мл у детей в возрасте от 1 года до 10 лет. При генерализованных синдромах мальабсорбции, таких, как целиакия, можно обнаружить пограничные цифры, несмотря на то что в их основе лежит дефицит фолата. При истинном дефиците В12, например при пернициозной анемии, уровень В12 сыворотки при первом обращении к врачу обычно значительно ниже 100 пг/мл. При дефиците ТК-I уровень В12 сыворотки низкий, а при дефиците ТК-II он нормальный.
Уровень фолата в сыворотке нормальный или повышенный при изолированном дефиците В12, но, как ни парадоксально, уровень эритроцитарного фолата низок при дефиците В12, так же как и при дефиците фолата, возможно, потому, что, как упоминалось выше, в клетки поступает зависимый от В12 5-метилтетрагидрофолат. Таким образом, результаты определений низкого уровня эритроцитарного фолата недостаточно показательны, но этого можно избежать, если последовательно ставить пробы на сывороточный В12 и сывороточный фолат (натощак).
Показателем дефицита В12, как первоначально установили Кокс и Вайт, может служить также экскреция метилмалоновой кислоты. Нагрузка валином увеличивает экскрецию и тест становится более чувствительным. Грин и Пегрум предложили практические модификации, которые позволяют проводить тест быстрее и делают его удобным для обычных патологических лабораторий. Взрослые получают нагрузку 10 г валина, и экскреция метилмалоновой кислоты более 40 мг в сутки указывает на дефицит В12. В педиатрии этот тест может быть использован при исследовании метаболизма лишь в особых случаях. В редких случаях метилмалоновой ацидурии, описанной Леви и соавторами, происходит метаболическая блокада без сопутствующих гематологических изменений.
Всасывание В12 лучше всего исследовать с помощью теста Шиллинга с В12, меченным 57Со, который больной принимает внутрь с добавлением нормального желудочного сока или ВФ и без них. Это означает, что в организм приходится вводить радиоактивный изотоп, поэтому такой тест нежелателен у детей младшего возраста, его используют только для особых исследовательских целей. Однако он позволяет точно разграничить отсутствие ВФ и нарушенное всасывание комплекса ВФ — В12, например, при избирательной мальабсорбции В12 у больных с синдромом Иммерсланда. В этой работе описаны члены одной семьи, достигшие возраста 15, 16 лет и 21 года к тому времени, когда был поставлен тест Шиллинга.
Дефицит В12 и фолата вызывает совершенно одинаковые гематологические последствия, включая не только макроцитоз и мегалобластную анемию, но в тяжелых случаях также нейтропению и тромбоцитопению. Клинические признаки — это бледность, болезненность и гладкая поверхность языка, а также такие общие явления, как гипотрофия и недостаточная прибавка массы у грудных детей, иногда сопровождаемые поносом и рвотой.
Если начать лечение с малых, «физиологических», доз фолиевой кислоты и В12, часто удается различить два типа дефицита. Взрослые с анемией, вызванной дефицитом фолиевой кислоты, дают хорошую реакцию на введение 0,2 мг фолиевой кислоты внутримышечно (от 1,3 до 7 мкг/кг) в сутки, причем оптимальная ретикулоцитарная реакция и нормобластоз костного мозга достигаются через 8-10 дней. В некоторых случаях дефицита В12 введение его в дозе от 0,3 до 0,4 мг в сутки может дать слабый эффект, но после дальнейшего введения внутримышечно 3 мкг в сутки сразу после курса фолиевой кислоты наблюдается оптимальная реакция. У детей эффективна соответственно меньшая доза В12 внутримышечно; так, например, 0,1 мкг в сутки вызывает полную гематологическую реакцию у грудных детей с дефицитом витамина В12.
Ребенок рождается с более высоким уровнем витамина В12 в сыворотке, чем у матери, даже если у нее имеется дефицит, хотя существует некоторая корреляция с уровнем В12 у матери. У нормальных грудных детей резервы в печени составляют 20-25 мкг, но у детей, родившихся от матерей с дефицитом витамина B12, они могут составлять всего 2-4 мкг. Уровень сывороточного В12 у 10 недоношенных детей наблюдался в динамике, и обнаружилось, что он постепенно снижается с первоначально нормальных или высоких величин и достигает минимума примерно к 40-му дню. У 5 детей уровень сывороточного В12 упал ниже 200 пг/мкл и у одного ребенка он достиг 77 пг/мкл. В дальнейшем уровни В12 самостоятельно вернулись к норме. Предполагалось, что эти изменения обусловлены низким поступлением В12, в то время когда потребность в нем увеличена.
Женское молоко содержит в среднем 0,11 мкг витамина В12 на 100 мл и. таким образом, может быть источником примерно 0,5 мкг В12. Содержание В12 в коровьем молоке выше. При дефиците В12 у матери концентрация его в молоке такая же, как в сыворотке крови, и ребенок получает ежедневно меньше 1/10 нормального количества, т. е. меньше 0,05 мкг в сутки.
Предполагается, что взрослые нуждаются в 2-5 мкг в сутки, потребность грудных детей неизвестна. Миктур и соавторы предположили, что у ребенка с массой тела 3 кг эта потребность составляет 0,04 мкг в сутки. Однако они просто рассчитали эту цифру на массу, приняв потребность взрослого с массой тела 70 кг равной 1 мкг. Бэкер и соавторы, рассуждая аналогичным образом, называют цифру 0,06 мкг в сутки. Ввиду того что в период быстрого роста потребность, вероятно, повышена, количество 0,04 мкг недостаточно. У многих детей с врожденным дефицитом внутреннего (фактора, у которых следовало бы ожидать при рождении нормального резерва В12 в 20-25 мкг, в возрасте 8-12 месяцев развивается мегалобластная анемия. Поэтому средняя потребность на первом году жизни, возможно, ближе к 0,1 мкг в сутки. Именно эта суточная пероральная доза может вызвать полную гематологическую реакцию в грудном возрасте.
Дефицит витамина В12 очень редко встречается в педиатрической практике и его легко не заметить, если не определять сывороточный В12 во всех случаях мегалобластной анемии. Системный дефицит возникает вследствие нарушенного всасывания или дефицита в пище, например, у детей, вскармливаемых грудью, матери которых страдают дефицитом витамина В12. Тканевой дефицит может возникнуть вследствие редкого дефекта транспортного механизма, т. е. дефицита ТК-II. Мальабсорбция витамина В12 у детей разделяется на три типа:
1) изолированное врожденное отсутствие внутреннего фактора при нормальной в других отношениях функции желудка; при этом мегалобластная анемия обычно развивается до возраста 2 лет;
2) пернициозная анемия, подобная этой же болезни у взрослых, с атрофией желудка и антителами против внутреннего фактора в сыворотке; однако она развивается на 2-м десятилетии жизни. У части детей этой последней категории имеются множественные эндокринные нарушения;
3) мальабсорбция при нормальной секреции внутреннего фактора вследствие генерализованного нарушения всасывания, обширных операций на кишечнике или кишечной патологии либо семейного избирательного дефекта всасывания витамина B12 в подвздошной кишке, сопровождаемого доброкачественной протеинурией.
Больных с системным дефицитом, вызванным нарушением всасывания, можно поддерживать в состоянии гематологической: ремиссии относительно небольшими парентеральными дозами витамина В12, например 100 мкг в месяц, но больные с дефицитом ТК-II нуждаются в значительно больших и более частых дозах, например 1000 мкг 2 раза в неделю.
Дефицит внутреннего фактора. В литературе описано менее 50 случаев. Мичурин и соавторы предполагали, что их можно разделить на два типа. У большинства больных с первым типом дефицита мегалобластная анемия развивается до возраста 2 лет (случай 4) и наблюдается изолированный дефицит внутреннего фактора при нормальной гистологии желудка или нормальной секреции кислоты без появления сывороточных антител к внутреннему фактору. Артур описал девочку 3 лет с дефектом этого типа. Гемоглобин составлял 4,8 г%, костный мозг был мегалобластный, уровень витамина В12 сыворотки был 60 пг/мл, а фолата в сыворотке — 17 мкг/мл. Тест Шиллинга показал нарушенное всасывание витамина В12, которое было нормализовано при введении внутреннего фактора. Внутренний фактор в желудке отсутствовал, но биопсия желудка дала нормальные результаты, не было признаков гастрита и атрофии. Как по росту, так и по массе тела девочка была ниже трех сигмальных отклонений от среднего уровня, но, после того как было начато парентеральное лечение цианокобаламином, рост резко активизировался.
Наблюдается большая частота семейных заболеваний у сиблингов, но, по-видимому, этот вид ювенильной пернициозной анемии те связан со взрослой формой пернициозной анемии.
Вторая, менее многочисленная группа больных, описанная Мичуриным, включает детей старшего возраста, обычно 10 лет и старше, у которых, помимо перечисленного, наблюдаются гистаминоустойчивая ахлоргидрия, атрофия слизистой желудка и антитела к внутреннему фактору. Предполагалось, что эти дети страдают такой же болезнью, что и пернициозная анемия взрослых, но, помимо многих общих признаков, существуют и.некоторые отличия. К ним относится большая частота эндокринных нарушений у детей, включая идиопатический гипопаратиреоз, болезнь Аддисона, гипотиреоз, полиэндокринопатию, ювенильный цирроз, недостаточность яичников, агенезию селезенки и иммунологические нарушения у больных и членов их семей. По-видимому, эти сопутствующие нарушения обусловлены генетически детерминированной тенденцией к образованию органоспецифических антител. Нарушения функции желудка совершенно такие же, как при аддисоновой пернициозной анемии у взрослых, но причина болезни, возможно, другая. Наследование, вероятно, рецессивное.
Избирательная мальабсорбция В12 в подвздошной кишке. Совершенно иной семейный синдром, вызванный изолированным дефектом кишечного всасывания В12 с нормальной кислотностью желудочного сока, нормальной гистологией и внутренним: фактором желудка, но с сопутствующей постоянной протеинурией был описан Имурсландом и соавторами. Вместе с более новыми сообщениями было описано 37 детей обоего пола в возрасте от 7 месяцев до 14 лет, но обычно младше 2 лет. У этих детей, по-видимому, имеется изолированный дефект всасывания комплекса внутреннего фактора с В12. после того как последний соединяется с клеточной поверхностью подвздошной кишки и до связывания В12 ТК-II. Других дефектов кишечного всасывания нет, и, согласно данным световой и электронной микроскопии, слизистая подвздошной кишки нормальна. Выявлена семейная тенденция в заболеваемости: так, дефект обнаружен у 3 братьев, но у обоих родителей всасывание было нормальным. Парентеральное введение B12 (100 мкг В12 в месяц) снимает мегалобластную анемию, но не ликвидирует протеинурию. Кроме того, описана протеинурия у годовалого больного, а анемия развилась у него спустя 10 лет.
Другие причины мальабсорбции. Слепые петли, анастомозы и свищи, созданные во время хирургических операций, могут быть связаны с нарушенным всасыванием В12, очевидно, вследствие изменения бактериальной кишечной флоры. Лечение тетрациклином может вызвать гематологическую ремиссию. Кишечная склеродермия также может сопровождаться мегалобластной анемией вследствие нарушенного всасывания В12 по аналогичной причине. Обширная резекция дистального отдела тонкого кишечника после гангрены на почве заворота в возрасте 20 дней привела к развитию мегалобластной анемии с низким уровнем сывороточного В12 в 11-месячном возрасте. Даллман и Диамонд описали ребенка, у которого через 36 ч после рождения была произведена тотальная резекция подвздошной кишки по поводу атрезии кишечника, а позднее, в возрасте 3 лет 4 месяца, у него развились дефицит В12 и мегалобластная анемия. Как и у взрослых, заражение широким лентецом может вызвать дефицит В12, так как паразит конкурирует с хозяином из-за витамина.
Дефицит В12 как проявление синдрома целиакии наблюдается редко; только у 1 из 19 детей с целиакией сывороточный В12 был низким. Вероятно, дефицит возникает чаще при тропической спру, так как кишечник при этом заболевании поражается на большем протяжении. У детей с фиброзным кистозом поджелудочной железы отмечена мальабсорбция кристаллического B12, но не пищевого, связанного с белком. Однако системного дефицита В12 не возникало.
Дефицит транскобаламина II. Раннее развитие глубокой мегалобластной анемии с нейтропенией, тромбоцитопенией, склонностью к инфекциям, гипотрофией, поносом, рвотой, красным воспаленным языком и язвами в полости рта описано у двух сибсов с дефицитом белка, транспортирующего В12 (ТК-II). Картина эта развернулась в возрасте 3 и 5 недель, хотя уровень гемоглобина при рождении был нормальным. Полная клиническая и гематологическая ремиссия была вызвана большими дозами введенного парентерально витамина B12 — 1000 мкг 2 раза в неделю или 500 мкг через день. Фолиевая кислота была неэффективна. Прекращение лечения витамином В12 у одного ребенка привело к рецидиву мегалобластной анемии через 6 мес. У этих двух детей сывороточный уровень В12 составлял 267 и 855 пг/мл, а у одного из них сывороточный фолат — 20 нг/мл. Всасывание В12 было снижено, причем введение внутреннего фактора не восполняло этого дефекта, следовательно, можно было предполагать, что ТК-II участвует в нормальном всасывании В12. У обоих родителей и у ряда других членов семьи, несмотря на гематологически нормальный статус, определялся низкий уровень ТК-II, что указывает на аутосомно-рецессивный тип наследования.
Различные белки, связывающие В12, идентифицируются при помощи ионообменной хроматографии на ДЭАЭ-целлюлозе или сывороточного электрофореза на полиакриламидном геле после уравновешивания В12. Когда сыворотка этих больных или здоровых лиц инкубируется с очень высокими концентрациями В12, появляются вторичные «пики» связывания. Возможно, что эти вторичные связывающие факторы начинают действовать, когда вводятся большие лечебные дозы В12, и заменяют нормальный ТК-II в его функции транспорта В12 в ткани.
Для изучения подобных нарушений можно воспользоваться еще одним тестом — измерять способность ненасыщенной сыворотки связывать витамин В12. Для этого меченный В12, добавляют к сыворотке при комнатной температуре и измеряют количество, которое может быть удалено при контакте с древесным углем, покрытым гемоглобином. Как и следует ожидать, при дефиците ТК-II связывающая способность снижена.
Недавно в Швейцарии описана еще одна семья с этим нарушением. Первоначальные признаки болезни заключались преимущественно в повышенной склонности к инфекции, связанной с агаммаглобулинемией и нарушенной продукцией антител.
источник
Витамин В12 является производным кобаламина (в основном, животного происхождения); кобаламины продуцируются в организме животных микроорганизмами. Человеческий организм не способен синтезировать витамин В12. Кобаламины выделяются в кислой среде желудка, где они соединяются с R-белками и внутренним фактором (ВФ), проходят через двенадцатиперстную кишку, где R-белки расщепляются протеазой поджелудочной железы и всасываются в дистальном отделе подвздошной кишки с помощью специфических рецепторов к комплексу ВФ + кобаламин. Кроме того, некоторое количество витамина В12, принимаемого в больших дозах, может диффундировать через слизистую оболочку полости рта и кишечника.
В плазме кобаламин связывается с транспортным белком, транскобаламином II (TK-II), который переносит витамин В12 в печень, костный мозг и другие места накопления. ТК-И входит в клетки путем рецепторно-опосредованно-го эндоцитоза и преобразуется в активные формы (метилкобаламин и аденозилкобаламин), которые играют важную роль в перемещении метальных групп и синтезе ДНК. Кроме того, плазма содержит также два других витамин В12-связывающих белка — транскобаламин I и транскобаламин III (TK-I и ТК-III). Эти формы транскобаламина не участвуют в транспорте, но отражают запас витамина В12 в тканях. Фактически почти весь витамин В12 в плазме связан с TK-I и ТК-Ш, и поэтому измерение концентрации В12 в сыворотке крови дает представление о запасах этого витамина в организме. В отличие от фолатов, витамин В12 способен накапливаться у детей старшего возраста и у взрослых в количестве, которого хватает на 3-5 лет. Однако у маленьких детей, рожденных от матерей с низким запасом витамина В12, клинические признаки дефицита кобаламина могут появиться в первые 4-5 мес. жизни.
Дефицит витамина В12 может быть результатом недостаточного поступления витамина с пищей, отсутствия секреции ВФ в желудке, пониженного всасывания комплекса ВФ + кобаламин в кишечнике или отсутствия белков для транспорта витамина В12.
Недостаточное поступление витамина В12. Поскольку витамин В12 присутствует во многих пищевых продуктах, алиментарный дефицит этого витамина — редкое явление, наблюдаемое при строго ограниченной диете (у строгих вегетарианцев), полностью лишенной животных продуктов.
Дефицит витамина В12 не наблюдается при квашиоркоре или младенческой дистрофии. У детей мегалобластная анемия развивается при недостаточном поступлении витамина В12 при грудном вскармливании младенца матерью-вегетарианкой или больной пернициозной анемией. Материнская пернициозная анемия может проявляться снижением концентрации витамина В12 в крови при наличии макроцитарной анемии у матери или без нее. Этот фактор часто является причиной мегалобластной анемии в течение первого года жизни.
Отсутствие внутреннего фактора. Врожденная пернициозная анемия — редкое заболевание с аутосомно-рецессивным типом наследования, причиной которого является неспособность к секреции желудочного ВФ или секреция функционально аномального ВФ. Она отличается от типичного заболевания у взрослых тем, что у детей желудок адекватно секретирует кислоту и является гистологически нормальным. Антитела к париетальным клеткам отсутствуют, а следовательно, и сопутствующие эндокринные нарушения. Симптомы ювенильной пернициозной анемии становятся очевидными в возрасте примерно около года. До этого времени организм живет за счет использования запасов витамина В12, сформированных во время внутриутробного развития. По мере усугубления анемии появляются слабость, раздражительность, отсутствие аппетита и вялость. Язык гладкий, красный и болезненный. Неврологические проявления включают атаксию, парестезии, снижение рефлексов, появление реакции Бабинского и мышечный клонус. Другим редким заболеванием является ювенильная пернициозная анемия, которая бывает у детей старшего возраста.
Это иммунологическое нарушение, похожее на пернициозную анемию взрослых. Признаки могут включать атрофию слизистой оболочки желудка, ахлоргидрию и наличие в сыворотке антител к ВФ и париетальным клеткам. У таких детей развиваются дополнительные иммунологические аномалии, кожный кандидоз, гипопаратиреоз и другие эндокринные расстройства. Аномальный результат пробы Шиллинга корригируется добавлением экзогенного ВФ. Такие пациенты время от времени нуждаются в парентеральном введении витамина В12. Дефицит ВФ может возникнуть после хирургической операции на желудке, и восприимчивые люди нуждаются в дополнительном пожизненном парентеральном введении витамина В12.
Нарушение всасывания витамина В12. У пациентов с воспалительными заболеваниями, такими как, например, регионарный энтерит (болезнь Крона), неонатальный некротизирующий энтероколит, может быть нарушено всасывание витамина В12. После хирургического удаления терминального отдела подвздошной кишки пациент нуждается в пожизненном введении витамина В12, если у него имеются признаки нарушения всасывания витамина. Причиной дефицита витамина В12 может быть чрезмерный рост кишечных бактерий в дивертикулах или дупликатурах тонкого кишечника, которые поглощают витамин, развертывают конкуренцию за него или расщепляют комплекс витамин + ВФ. В этих случаях соответствующее лечение антибиотиками дает гематологическую реакцию. Аналогичные механизмы действуют при инвазии верхней части тонкого кишечника ленточным червем Di-phylobotrium latum. Мегалобластная анемия, которая развивается в этих случаях, характеризуется пониженным уровнем витамина В12 в сыворотке крови, наличием ВФ в желудочном соке и тем, что аномальный результат пробы Шиллинга не корригируется добавлением экзогенного ВФ.
Описаны редкие случаи семейного отсутствия или дефекта рецептора для комплекса ВФ + витамин В12 в терминальных отделах подвздошной кишки, которые иногда связаны с протеинурией (синдром Имерслунд-Гресбека). Пониженная активность рецепторов может обнаруживаться в моче пациентов с помощью метода присоединения радионуклидов.
Гистологически желудок нормальный, в желудочном секрете присутствуют ВФ и кислота. Данный вид нарушения с аутосомно-доминантным типом наследования вызывается дефектом гена CUBN на хромосоме Юр 12.1, результатом чего является уменьшение экспрессии рецептора для комплекса ВФ + В12. Дефицит корригируется ежемесячным парентеральным введением витамина В12. Отсутствие транспортного белка витамина В12. Дефицит ТК-И является редкой причиной мегалобластной анемии, которая обусловлена в этом случае снижением утилизации кобаламина.
TK-II является главным физиологическим переносчиком витамина В12. ТК-И играет такую же роль в транспорте В,2, как и трансферрин в транспорте железа; клетки, которые нуждаются в В12 или железе, имеют специфические рецепторы для ТК-И или трансферрина. Наследственный дефицит передается аутосомно-рецессивным путем и выражается в неспособности всасывать или транспортировать B12.
источник
- Общественная организация Национальное общество детских гематологов
- онкологов
- ФГБУ «ФНКЦ ДГОИ им. Дмитрия Рогачева» Минздрава России
- НКЦ ГОИ
- РГМУ им. акад И.П. Павлова.
1.1 Определение
Анемия – состояние, при котором снижается общее количество гемоглобина в организме. Снижение концентрации гемоглобина в крови является ключевым показателем, поскольку может быть измерено напрямую.
1.2 Этиология и патогенез
Основные причины развития витамин-В12-дефицитной анемии:
Снижение поступления витамина В12 с питанием (у грудных детей, чьи матери имеют дефицит витамина В12, строгая вегетарианская диета)
Снижение всасывания (дефицит внутреннего фактора Кастла, резекция желудка, нарушение всасывания в подвздошной кишке вследствие болезней тонкого кишечника, резекции кишечника)
Повышенные потери в кишечнике (глистная инвазия, синдром слепой кишки)
Нарушение транспорта витамина В12 из кишечника в ткани (наследственный дефицит транскобаламина)
Синдром Иммерслунд-Гресбек – сочетание протеинурии с нарушением всасывания комплекса витамина В12 и внутреннего фактора в тонком кишечнике, редкое заболевание, обусловленное мутацией генов и дебютирующее в раннем детстве.
Цианкобаламин (витамин В12) содержится в пищевых продуктах животного происхождения (мясе, рыбе). Запасы витамина В12 в организме взрослого человека составляют около 5 мг, и если учесть, что за сутки теряется около 5 мкг, то полное истощение запасов при отсутствии поступления (нарушение всасывания, вегетарианская диета) наступает только через 3 года.
Однако существует ряд причин, которые могут привести к развитию острой витамин В12 дефицитной анемии: 1) длительный наркоз закисью азота [3], 2) тяжелые заболевания с массивными трансфузиями, диализом, полным парентеральным питанием.
Цианкобаламин в желудке связывается с внутренним фактором — гликопротеином, продуцируемым париетальными клетками желудка и другими связывающими белками, присутствующими в слюне и желудочном соке. Эти комплексы предохраняют цианкобаламин от разрушения при транспорте по ЖКТ. В подвздошной кишке комплекс внутреннего фактора с цианкобаламином связывается со специфическими рецепторами на поверхности эпителиальных клеток, освобождение цианкобаламина из клеток кишечного эпителия и транспорт в ткани происходит с помощью особых белков плазмы крови – транскобаламинов. В клетках витамин В12 является кофактором метилтрасферазной каталитической реакции, осуществляющей ресинтез метионина и одновременно регенерацию 5-метилтетрагидрофолата в тетрагидрофолат и 5,10 метилентетрагидрофолат.
Дефицит витамина В12 может быть вызван плохим питанием, нарушенным всасыванием (врожденный или приобретенный дефицит внутреннего фактора, дефект рецептора к комплексу витамина В12 и внутреннего фактора в тонком кишечнике при синдроме Иммерслунд-Гресбек, кишечные заболевания) или нарушением метаболизма (врожденная ферментная патология, дефицит транскобаламина, воздействие закиси азота).
Недостаточное поступление витамина В12 с пищей редко встречается у детей, хотя может наблюдаться у грудных детей, чьи матери сами имеют дефицит витамина В12. Пернициозная анемия, которая обычно является причиной дефицита витамина В12 у взрослых, редко встречается у детей. Наиболее частой причиной дефицита витамина В12 у детей является нарушение всасывания и врожденный дефицит белков-переносчиков.
1.3 Эпидемиология
Данных о распространенности дефицита витамина В12 и витамин В12 дефицитной анемии у детей в России нет.
1.4 Кодирование по МКБ-10
Витамин-B12-дефицитная анемия (D51):
D51.0 — Витамин-B12-дефицитная анемия вследствие дефицита внутреннего фактора;
D52.1 — Витамин-B12-дефицитная анемия вследствие избирательного нарушения всасывания витамина B12 с протеинурией;
D52.2 — Дефицит транскобаламина II;
D52.3 — Другие витамин-B12-дефицитные анемии, связанные с питанием;
D51.8 — Другие витамин-B12-дефицитные анемии;
D51.9 — Витамин-B12-дефицитная анемия неуточненная.
2.1 Жалобы и анамнез
Рекомендовано выяснить характер питания пациента. В случае грудных детей следует выяснить характер питания матери, уточнить, как она питалась до беременности, во время беременности и во время кормления грудью.
Дети, в питании которых недостаточно витамина В12, с большой вероятностью имеют дефицит других питательных веществ (в том числе фолиевой кислоты, железа).
Необходимо обратить внимание на возможные проявления синдрома мальабсорбции. Выяснить наличие в анамнезе резекции желудка, резекции тонкого кишечника с формированием синдрома слепой кишки. Необходимо исключить инвазию широким лентецом. Исключить болезнь Крона и другие причины хронического воспаления в подвздошной кишке.
Наследственное отсутствие или нехватка белков-переносчиков является важной причиной дефицита витамина В12. Необходимо собрать подробный семейный анамнез. Данная патология часто дебютирует в раннем детстве и при отсутствии лечения может быть причиной не только анемии, но и миелопатии и задержки развития [1,2].
Необходимо исследование мочи для исключения протеинурии, как проявления синдрома Имерслунд-Грэсбек [4].
Для клиники дефицита витамина В12 характерна триада:
— поражение крови;
— поражение ЖКТ;
— поражение нервной системы.
Анемия появляется слабостью, быстрой утомляемостью, одышкой, сердцебиением. В результате повышенного разрушения эритроидных клеток (неэффективный эритропоэз) развивается умеренная желтуха за счет непрямого билирубина. Поражение ЖКТ проявляется анорексией, глосситом, «лакированным» языком. Выявляется снижение желудочной секреции, атрофический гастрит. В результате поражения периферической нервной системы (фуникулярный миелоз) появляются атаксия, парестезии, гипорефлексия, рефлекс Бабинского, в тяжелых случаях – клонус и кома. У детей раннего возраста развиваются гипотрофия, отставание в росте, раздражительность, хроническая диарея, склонность к инфекциям. Если неврологические симптомы выявляются, их динамику необходимо оценить на фоне лечения.
2.2 Физикальное обследование
Общий осмотр подразумевает оценку общего физического состояния, роста и массы тела. Выявляется бледность кожных покровов, слизистых, при тяжелой анемии присутствует учащенное сердцебиение, одышка.
Поскольку при витамин В12 дефицитной анемии в костном мозге происходит неэффективный эритропоэз и за счет этого повышенное разрушение гемоглобинсодержащих клеток, в крови повышается уровень непрямого билирубина и появляется легкая желтушнось склер и кожи. При тяжелых формах может наблюдаться небольшое увеличение селезенки (реактивная гиперплазия).
При обследовании выявляется упомянутая выше патология желудочно-кишечного тракта (глоссит, атрофический гастрит) и неврологические симптоматика (фуникулярный миелоз).
2.3 Лабораторная диагностика
Для витамин В12 дефицитной анемии характерны:
-низкий уровень ретикулоцитов;
-высокий уровень сывороточного железа;
-высокий уровень ферритина;
-умеренное повышение непрямого билирубина;
-нормальный уровень фолата в сыворотке крови (более 3 нг/мл);
-нормальный уровень фолата в эритроцитах;
-низкий уровень витамина В12 в крови (менее 100 пг/мл);
-картина мегалобластического кроветворения в костном мозге.
- Рекомендован общий анализ крови с микроскопией мазка крови
Уровень достоверности доказательств 1 (уровень убедительности рекомендаций В)
Комментарии: При сочетании дефицита железа и витамина В12 могут наблюдаться сочетания лабораторных признаков, что приводит к неопределенной картине и затруднению диагностики; в этом случае надо ориентироваться на клинические симптомы и анамнез.
Высокий ретикулоцитоз может являться признаком продолжающегося кровотечения, гемолиза, а также наблюдается при витамин В12 дефицитной анемии через неделю после назначения витамина В12.
Наряду с анемией, как правило, отмечается умеренное снижение уровня тромбоцитов и лейкоцитов.
При наличии двух- или трехростковой цитопении необходимо рассмотреть необходимость исследования костного мозга для исключения лейкемии, миелодиспластического синдрома, апластической анемии.
Характерные признаки мегалобластического кроветворения в костном мозге исчезают через несколько часов после инъекции витамина В12 [1,2].
- Рекомендован биохимический анализ крови.
Уровень достоверности доказательств 1 (уровень убедительности рекомендаций В)
- Рекомендовано исследование уровня сывороточного железа, ферритина, фолиевой кислоты и витамина В12 в крови.
Уровень достоверности доказательств 3 (уровень убедительности рекомендаций С)
Рекомендовано исследование мочи для исключения протеинурии, характерной для синдрома Иммерслунд-Гресбек [4].
Уровень достоверности доказательств 4 (уровень убедительности рекомендаций D)
- Рекомендовано проводить исследование всасывания Витамина В12 в кишечнике
Уровень достоверности доказательств 4 (уровень убедительности рекомендаций D)
Комментарии: Нарушение всасывания витамина В12 в кишечнике можно диагностировать с помощью теста Шиллинга с радиоактивным меченым витамином В12. Учитывая недоступность меченого витамина В12 в общей лабораторной практике можно использовать модифицированный тест Шиллинга: после приема внутрь витамина В12 определяется уровень витамина в крови. Отсутствие повышения уровня витамина В12 указывает на нарушение всасывания витамина в кишечнике.
2.4 Дифференциальная диагностика
Дифференциальный диагноз проводят с фолиеводефицитной анемией, другими формами анемии с мегалобластоидным типом кроветворения: врожденной оротатацидурией, синдром Леша-Найена (Lesch-Nyhan), тиамин-зависимой мегалобластной анемией, врожденной дизэритропоэтической анемией, эритролейкемией. Кроме того, необходимо исключить формы анемии, протекающие с макроцитозом, но без признаков мегалобластоидности – апластическую анемию, аутоиммунную гемолитическую анемию, заболевания печени, гипотиреоз, сидеробластные анемии.
Необходимо оценить размеры лимфатических узлов, печени, селезенки, исключить наличие образований в брюшной полости, забрюшинном пространстве, другие признаки злокачественных заболеваний.
Показания к лечению в стационаре: анемия тяжелой степени. В остальных случаях лечение проводится в амбулаторных условиях.
- Рекомендовано проведение заместительной терапии витамина В12.
Уровень достоверности доказательств 1 (уровень убедительности рекомендаций А)
Комментарии: Витамин В12 назначается в дозе 5 мкг/кг в день детям в возрасте до одного года, 100—200 мкг в день детям после года, 200—400 мкг в день подросткам. Курс лечения составляет 4 недели. Поддерживающая терапия: еженедельное введение препарата в той же дозе в течение 2 мес, затем последующие 6 мес препарат вводится 2 раза в месяц. При невозможности устранить причину развития анемии противорецидивные курсы лечения витамином В12 проводятся ежегодно, на один курс 10—15 инъекций [1,2,5]
У отдельных пациентов на фоне лечения витамином В12 и активизации эритропоэза может проявиться дефицит железа, который препятствует полной нормализации показателей крови и требует стандартного лечения препаратами железа.
- При снижении уровня гемоглобина ниже 50 г/л, тяжелых инфекциях, сердечно-сосудистых нарушениях рекомендовано переливание эритроцитной массы.
Уровень достоверности доказательств 2 (уровень убедительности рекомендаций В)
- Рекомендовано проводить контроль показателей крови в процессе лечения.
Уровень достоверности доказательств 4 (уровень убедительности рекомендаций D)
Комментарии: Необходимо проводить общий анализ крови с подсчетом ретикулоцитов, тромбоцитов, гематокрита — на 7 — 10 день от начала лечения. Наличие ретикулоцитарной реакции является важным признаком правильности лечения. Так же необходим контроль показателей крови 1 раз в неделю. Нормализация уровня Hb происходит через 4 — 6 недель от начала лечения и является решающим подтверждением правильности диагноза и лечения.
Специфических реабилитационных мероприятий в отношении пациентов с витамин В12 дефицитной анемией нет. Диспансерное наблюдение проводится с учетом возможности или невозможности устранения причины дефицита витамина В12.
Первичная профилактика заключается в рациональном питании, своевременной диагностике и лечении глистных инвазий, назначении витамина В12 при состояниях, ведущих к развитию его дефицита (например, после резекции кишечника, субтотальной резекции желудка).
Критерии качества
Уровень достоверности доказательств
Уровень убедительности рекомендаций
Выполнен общий (клинический) анализ крови развернутый
Выполнен анализ крови биохимический (общетерапевтический)
Проведена терапия препаратами витамина В12
Детская гематология/ Под ред: А.Г. Румянцева, А.А. Масчана, Е.В. Жуковской. Москва. Издательская группа « ГЭОТАР Медиа» 2015 г. С. 656
Whitehead VM. Acquired and inherited disorders of cobalamin and folate in children. Br J Haematol. 2006 Jul. 134(2):125-36.
Duma A, Cartmill C, Blood J, Sharma A, Kharasch ED, Nagele P. The hematological effects of nitrous oxide anesthesia in pediatric patients. Anesth Analg. 2015 Jun. 120 (6):1325-30.
Dugu? B, Ismail E, Sequeira F, Thakkar J, Gr?sbeck R. Urinary excretion of intrinsic factor and the receptor for its cobalamin complex in Gr?sbeck-Imerslund patients: the disease may have subsets. J Pediatr Gastroenterol Nutr. 1999 Aug. 29(2):227-30
Trakadis YJ, Alfares A, Bodamer OA, et al. Update on transcobalamin deficiency: clinical presentation, treatment and outcome. J Inherit Metab Dis. 2014 May. 37 (3):461-73
Румянцев А.Г. доктор медицинских наук, профессор, главный детский гематолог Министерства здравоохранения Российской Федерации, директор Федерального научно-клинического центра детской гематологии, онкологии и иммунологии им. Дмитрия Рогачёва , член правления Союза педиатров России, академик РАМН.
Масчан А.А. д.м.н., зам. генерального директора ФГБУ ФНКЦ ДГОИ им. Дмитрия Рогачева, профессор кафедры гематологии, онкологии и лучевой терапии педиатрического факультета РНИМУ им. Н.И.Пирогова, президент Национального общества детских гематологов и онкологов, член Европейского общества гематологов.
Демихов Валерий Григорьевич — д.м.н., профессор, директор Научно-клинического центра гематологии, онкологии и иммунологии ГБОУ ВПО «Рязанский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России, член НОДГО, член Европейской гематологической ассоциации (EHA).
Скобин В.Б., к.м.н., врач-гематолог Научно-клинического центра гематологии, онкологии и иммунологии ГБОУ ВПО «Рязанский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России, член НОДГО.
Журина О.Н., к.м.н., зав. лабораторией Научно-клинического центра гематологии, онкологии и иммунологии ГБОУ ВПО «Рязанский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России, член НОДГО.
Конфликт интересов отсутствует.
Целевая аудитория данных клинических рекомендаций:
Таблица П1 – Уровни достоверности доказательств
Уровень достоверности
Источник доказательств
Проспективные рандомизированные контролируемые исследования
Достаточное количество исследований с достаточной мощностью, с участием большого количества пациентов и получением большого количества данных
Как минимум одно хорошо организованное рандомизированное контролируемое исследование
Репрезентативная выборка пациентов
Проспективные с рандомизацией или без исследования с ограниченным количеством данных
Несколько исследований с небольшим количеством пациентов
Хорошо организованное проспективное исследование когорты
Мета-анализы ограничены, но проведены на хорошем уровне
Результаты не презентативны в отношении целевой популяции
Хорошо организованные исследования «случай-контроль»
Нерандомизированные контролируемые исследования
Исследования с недостаточным контролем
Рандомизированные клинические исследования с как минимум 1 значительной или как минимум 3 незначительными методологическими ошибками
Ретроспективные или наблюдательные исследования
Серия клинических наблюдений
Противоречивые данные, не позволяющие сформировать окончательную рекомендацию
Мнение эксперта/данные из отчета экспертной комиссии, экспериментально подтвержденные и теоретически обоснованные
Таблица П2 – Уровни убедительности рекомендаций
Уровень убедительности
Расшифровка
Рекомендация основана на высоком уровне доказательности (как минимум 1 убедительная публикация I уровня доказательности, показывающая значительное превосходство пользы над риском)
Метод/терапия первой линии; либо в сочетании со стандартной методикой/терапией
Рекомендация основана на среднем уровне доказательности (как минимум 1 убедительная публикация II уровня доказательности, показывающая значительное превосходство пользы над риском)
Метод/терапия второй линии; либо при отказе, противопоказании, или неэффективности стандартной методики/терапии. Рекомендуется мониторирование побочных явлений
Рекомендация основана на слабом уровне доказательности (но как минимум 1 убедительная публикация III уровня доказательности, показывающая значительное превосходство пользы над риском) или
нет убедительных данных ни о пользе, ни о риске)
Нет возражений против данного метода/терапии или нет возражений против продолжения данного метода/терапии
Рекомендовано при отказе, противопоказании, или неэффективности стандартной методики/терапии, при условии отсутствия побочных эффектов
Отсутствие убедительных публикаций I, II или III уровня доказательности, показывающих значительное превосходство пользы над риском, либо убедительные публикации I, II или III уровня доказательности, показывающие значительное превосходство риска над пользой
Порядок обновления клинических рекомендаций – пересмотр 1 раз в 5 лет.
- Порядок оказания медицинской помощи населению по профилю «гематология» (утв. приказом Министерства здравоохранения Российской Федерации от 15 ноября 2012 г. № 930н).
Нехватка витамина В12 может наблюдаться у детей при редких заболеваниях: глистной инвазии широким лентецом, при редких врожденных заболеваниях, связанных с нарушением образования внутреннего фактора Кастла (белка, ответственного за перенос витамина В12 из пищи в кровь), а также иммунном заболевании, причиной которого является выработка антител к внутреннему фактору. Одной из причин может являться неправильное питание, строгая вегетарианская диета. При нехватке в организме витамина В12 развивается анемия, хронический гастрит, воспаление языка (глоссит), появляются неврологические нарушения. Заболевание легко поддается лечению витамином В12. Через месяц после начала лечения происходит нормализация уровня гемоглобина. Если причину дефицита витамина В12 можно устранить (глисты, неправильное питание), поддерживающее лечение не проводится. Если причину устранить невозможно (наличие антител к внутреннему фактору Кастла, врожденное отсутствие внутреннего фактора), поддерживающее введение витамина В12 проводится пожизненно. Самостоятельное использование препарата недопустимо. Назначить витамин В12 с учетом всех показаний и противопоказаний должен ваш врач.
источник