Состояние кишечника и его микрофлоры отражается на работе всего организма. Помимо функции пищеварения кишечник имеет и другие важные свойства. Одно из них — это синтез некоторых необходимых витаминов. Важно поддерживать здоровье кишечника и микрофлоры, так как именно от них зависит состояние иммунитета и даже внешний вид человека. Для чего нужны бактерии в кишечнике и какие витамины синтезируют бактерии в толстом кишечнике — важные темы для тех, кто заботится о своем здоровье.
В кишечнике людей насчитывается около 500 разновидностей бактерий, как полезных, так и вредных для здоровья. Общий вес бактерий может достигать 3-х килограммов. У здорового человека насчитывается примерно около 60% полезных микроорганизмов из общего количества. Поэтому если этот уровень падает, и болезнетворные бактерии начинают активно размножаться, падает иммунитет, человек болеет, появляются проблемы с пищеварением.
Микрофлора кишечника участвует в таких процессах:
- способствует нормализации перистальтики кишечника;
- вырабатывает иммуноглобулин, укрепляет иммунитет;
- подавляет рост патогенной микрофлоры;
- способствует детоксикации организма, повышает защиту от раковых клеток;
- участвует в синтезе биологически активных соединений и витаминов;
- регулирует обмен веществ.
Состав микрофлоры человека зависит от среды ее обитания, а именно кишечника. Какие бактерии будут активно размножаться в организме, зависит от общего состояния пищеварительных органов и от употребляемой человеком пищи. Патологические бактерии развиваются при наличии большого количества белковой пищи. Полезные микроорганизмы предпочитают растительные продукты с большим содержанием пищевых волокон, углеводов и полисахаридов. Поэтому без употребления овощей, фруктов и круп, в которых содержится много клетчатки, микрофлора в кишечнике не сможет эффективно противостоять патологическим микроорганизмам.
Рацион современного человека в большей степени состоит из рафинированных продуктов. Многие продукты питания содержат вредные пищевые добавки. В результате страдает микрофлора кишечника, что препятствует ей синтезировать и усваивать витамины.
Заболевания желудочно-кишечного тракта, дисбактериоз пагубно влияют на флору кишечника. Развитию патологических бактерий способствует прием некоторых лекарственных препаратов, особенно, антибиотиков. Лечение многими гормональными средствами и контрацептивами также вредит состоянию кишечника.
Употребление пребиотиков и пробиотиков способствует нормализации микрофлоры. Это, в свою очередь, повышает количество синтезированных витаминов и укрепляет иммунитет.
Пробиотики — это живые микроорганизмы, которые населяют кишечник. Они способствуют улучшению здоровья человека. Известными препаратами с пробиотиками являются Линекс, Бифидумбактерин Форте, Бифиформ.
Пребиотики — органические вещества, которые способствуют размножению полезных микроорганизмов в кишечниках. Содержатся в некоторых продуктах — молочная продукция, квашеная капуста, маринованные огурцы, хлеб, соевый соус, вино
Витамины жизненно необходимы для организма. Их дефицит отражается на работе всех органов. Некоторые витамины поступают только вместе с пищей, иные организм способен продуцировать сам. Например, некоторые полезные вещества выделяются в кишечнике человека. В синтезе витаминов в большей степени принимают участие микрофлора тонкого и толстого кишечника.
Какие витамины синтезируются микрофлорой кишечника:
- В12. Витамин, в небольшом количестве синтезирующийся в кишечнике, очень важен для здоровья человека. Он отвечает за метаболизм жиров, белков и углеводов и синтез ДНК и РНК, помогает в работе нервной системы. Гиповитаминозом В12 чаще страдают люди пожилого возраста, беременные женщины, при заболеваниях желудочно-кишечного тракта (ЖКТ), печени, а также курящие и злоупотребляющие алкоголем. Витамин относится к водорастворимым. Он не накапливается в организме, а микрофлора кишечника вырабатывает его в недостаточном количестве. Поэтому важно употреблять пищу, обогащенную этим веществом (телячья печень, лосось, говядина, баранина, большинство морепродуктов). Также недостаток витамина В12 будет ощущаться при дисбактериозе кишечника.
- В3. Без этого витамина в организме невозможны окислительно-восстановительные процессы, нормальная работа высшей нервной системы. Витамин имеет влияние на пищеварение, сердечно-сосудистую систему, положительно отражается на состоянии кровеносных сосудов, регулирует артериальное давление, понижает уровень холестерина и способствует очищению организма от токсинов. Этот витамин синтезируется микрофлорой кишечника при употреблении пищи с аминокислотой триптофаном и витаминами В2 и В6. Витамином богаты такие продукты: орехи, печень, мясо, яйца, бобовые, помидоры. А также картофель, кукуруза, гречка и овощи зеленого цвета.
- В9 (фолиевая кислота). За выработку и всасывание витамина отвечает тонкая кишка. Вещество принимает активное участие в процессе кроветворения, влияет на образование белых кровяных телец, регулирует работу печени, кишечника, укрепляет защитные силы организма. Известно, что без фолиевой кислоты нарушается обмен веществ, понижается деятельность головного мозга, страдает костный мозг. Крайне важно поддерживать нормальный уровень витамина беременным женщинам, так как он принимает участие в формировании нервной системы плода. Фолиевая кислота содержится в бобовых, фруктах и овощах, злаках, гречневой и овсяной крупах. А также цитрусах, яйцах, мясе, рыбе, молоке.
- К2. Витамин способствует выработке белка в костях, а также необходим для свертываемости крови. При его недостатке случаются кровотечения, присутствует кровь в кале, образовываются подкожные кровоизлияния. Если кишечник находится в здоровом состоянии, то витамин К вырабатывается в достаточном количестве, поэтому нет необходимости принимать дополнительные вещества. Человек испытывает недостаток в витамине при дисбактериозе и заболеваниях кишечника. Дополнительно витамин можно получить, употребляя шпинат, все виды капусты, отруби пшеницы, киви, бананы. А также молоко, мясо, яйца, оливковое масло.
В организме человека кишечник выполняет множество функций. Кроме переваривания пищи, орган способствует повышению иммунитета, защищает от развития раковых клеток. Также известно, что микрофлора синтезирует некоторые важные витамины, отвечает за процесс их усвоения. От состояния кишечника зависит общее здоровье организма. Правильное питание с преобладанием растительных пищевых волокон, употребление пробиотиков и пребиотиков способствует размножению полезных микроорганизмов, которые будут стоять на страже здоровья.
В видео ниже рассказывается, что такое дисбактериоз и как с ним бороться.
источник
«Мы есть то, что мы едим» (Гиппократ).
Статья на конкурс «био/мол/текст»: «Мы есть то, что мы едим». Так говорил Гиппократ. Но мог ли он себе представить, насколько он был прав? Судя по последним научным данным, потребляемая пища очень сильно влияет на нашу кишечную микрофлору, которая в конечном счете влияет на наш организм. Причем влияет вполне осязаемо — например, меняя наш вес! Получается замкнутый круг: человек — микрофлора — человек.
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2016.
Генеральным спонсором конкурса, согласно нашему краудфандингу, стал предприниматель Константин Синюшин, за что ему огромный человеческий респект!
Спонсором приза зрительских симпатий выступила фирма «Атлас».
Спонсор публикации этой статьи — Алексей Петрович Семеняка.
Давно известна роль кишечной микрофлоры в регуляции многих процессов организма. К примеру, она формирует защитный барьер слизистой оболочки кишечника, стимулирует иммунную систему [1], нейтрализует токсины, продуцирует витамины, переваривает клетчатку и многое-многое другое. Но наука, как известно, не стоит на месте, и появляются новые данные. Так, например, теперь рассматривается взаимосвязь между состоянием кишечной микрофлоры и ожирением, а также развитием сахарного диабета (СД) 2-го типа!
Напомним, что представляет собой нормальная микрофлора человека. Нормофлора (микрофлора в нормальном состоянии, или эубиоз) — это совокупность микробных популяций отдельных органов и систем, характеризующаяся определенным качественным и количественным составом и поддерживающая биохимическое и иммунологическое равновесие, необходимое для сохранения здоровья человека.
Кишечный микробиом, упоминаемый некоторыми авторами как отдельный орган, несет ответственность за метаболические процессы в организме (рис. 1). Бактерии инактивируют ферменты, гормоны, токсины, разлагают желчные кислоты, нейтрализуют аллергены, образуют молочную кислоту, что помогает пищеварению, способствуют всасыванию витаминов D и B12, кальция и железа в кишечнике, а также синтезируют витамины B1, B2, B6, B12, H, К, C, никотиновую, пантотеновую и фолиевую кислоты [2]. Микрофлора определяет в значительной степени не только физическую составляющую человеческой жизни, но и психическую. Обнаружено, что отходы жизнедеятельности бактерий могут непосредственно влиять на мозг. Например, как минимум два типа кишечных бактерий производят γ-аминомасляную кислоту (ГАМК) [3] — нейромедиатор, ответственный за своевременное гашение процессов возбуждения в центральной нервной системе, а возможно, и помогающий поддерживать нормальный сон и усваивать глюкозу [4]. А последние научные разработки касаются связи состава кишечной микробиоты с проявлением аутизма и депрессии.
Рисунок 1. Основные функции нормальной микрофлоры.
Метаболическая активность кишечной микробиоты, помимо удовлетворения собственных нужд бактерий, способствует извлечению калорий из потребляемой хозяином пищи, помогает запасать эту энергию в его жировых депо, то есть формировать жировую ткань. В экспериментах с гнотобиотическими (безмикробными) и заселенными определенными бактериями мышами было показано, что кишечная микрофлора обеспечивает разложение неперевариваемых хозяином полисахаридов пищи до усваиваемых форм — но это сложно назвать новостью. Находкой же стало то, что этот процесс сопровождался усилением всасывания моносахаридов из кишечника и их поступления в воротную вену — возможно, благодаря повышению плотности капиллярной сети в слизистой оболочке тонкой кишки под влиянием микробиоты. Это вело к усилению печеночного липогенеза, то есть синтеза жирных кислот из углеводов. Дело в том, что клетки печени реагируют на повышение уровня глюкозы и инсулина в крови экспрессией генов транскрипционных факторов ChREBP и SREBP-1, которые активируют гены биосинтеза триглицеридов, то есть жиров. Усиление выработки этих транскрипционных факторов и наблюдали после заселения мышиных кишечников микробиотой. Кроме того, кишечные бактерии помогали размещать новопроизведенные триглицериды в жировых клетках (адипоцитах), вмешиваясь в работу хозяйских генов: микрофлора увеличивала активность необходимой для этого липопротеинлипазы, подавляя в эпителии тонкого кишечника синтез ее ингибитора.
Однако здесь стоит напомнить, что речь шла о мышах, о конкретном энтеротипе их микрофлоры (биоценозе, в котором преобладают определенные группы бактерий) и вообще о базовых функциях микробиоты. Поэтому не нужно на основании этой работы делать вывод о вредном влиянии любых кишечных бактерий на хозяина, просто именно так появилась гипотеза о множественных и взаимосвязанных механизмах влияния кишечной микробиоты на энергетический обмен хозяина, а с ней и надежда на то, что коррекция этого влияния поможет справиться с эпидемией ожирения [5]. Авторы работы предположили, что микробный «биореактор» у одного индивида может быть более энергоэффективным, чем у другого. И факторы, влияющие на это, мы еще затронем.
Недавние эксперименты показали, что изменения микрофлоры относятся к причинам ожирения, а не к его следствиям. Если кишечник гнотобиотических мышей заселить микробиотой мышей с ожирением, животные будут набирать вес быстрее, чем в случае пересадки бактерий от худых мышей. Более того, по составу микробиоты можно с 90-процентной вероятностью предсказать, есть ли у человека ожирение [6]. Только представьте! А теперь вообразите, что, изменяя состав кишечной микрофлоры человека, можно будет регулировать его вес (рис. 2).
Рисунок 2. Чем примечателен состав микрофлоры кишечника тучного человека?
Многократно выявляли, что при ожирении увеличивается количество представителей типа Firmicutes (например, Clostridium coccoides, C. leptum) и семейства Enterobacteriaceae (Esherichia coli). В то же время снижается количество представителей типа Bacteroidetes (Bacteroides, Prevotella), сокращаются популяции бактерий родов Bifidobacterium и Lactobacillus [7]. Ранее было показано, что высокожировая диета способствует воспалению слизистой оболочки кишечника, опосредованному снижением численности лактобактерий. Это воспаление предрасполагает к развитию ожирения и инсулинорезистентности, то есть СД 2-го типа. В 2016 году в экспериментах с мышами удалось установить связь между этими состояниями и дефицитом конкретных штаммов Lactobacillus reuteri в пейеровых бляшках. Дело в том, что богатая жирами пища обеспечивает отбор бактериальных штаммов, устойчивых к окислительному стрессу. А такими оказались как раз лактобациллы, выделяющие провоспалительные цитокины. И наоборот, вытеснялись из популяции «хорошие» штаммы L. reuteri — продуценты противовоспалительных веществ [8].
Как уже упоминалось, анализ кишечного микробиома выявил резкое уменьшение доли Bacteroidetes и увеличение доли Firmicutes у мышей с наследственным ожирением по сравнению с обычными мышами [9]. Такие же изменения нередко наблюдали и у людей: в одном исследовании 12 пациентов с ожирением отличались от контрольной группы худых сниженным содержанием бактерий Bacteroidetes и повышенным — Firmicutes. Затем пациентов перевели на низкокалорийную диету (питание с ограничением жиров и углеводов) и в течение года следили за изменением состава их кишечной микрофлоры. Оказалось, что диета значительно сокращала численность Firmicutes и повышала долю Bacteroidetes, но самое главное — эти изменения коррелировали со степенью снижения массы тела [9]. Тем не менее взаимосвязь индекса массы тела с пропорцией Bacteroidetes/ Firmicutes пока нельзя назвать доказанной [10].
В рамках проекта MetaHIT, посвященного изучению кишечного метагенома, то есть совокупности геномов всех обитателей кишечника, было обследовано 124 европейца [11]. Суммарное количество генов кишечного микробиома в 150 раз (!) превышало количество генов человека. Но стоит отметить, что избыток жирной пищи вел к сокращению бактериального разнообразия: у тучных людей было в среднем на шесть видов бактерий меньше, чем у лиц с нормальной массой тела. Результаты метагеномного анализа разделили участников эксперимента на две группы: носителей «малого генома» (low gene count) и носителей «большого генома» (high gene count). Малый геном — это метагеном, в котором относительно мало генов различных видов бактерий: разница между «малым» и «большим» геномами по количеству генов достигала в среднем 40%. У большинства лиц с бедным кишечным метагеномом преобладали Bacteroides, а с богатым — Methanobrevibacter. При этом две описанные категории людей сильно различались представленностью в их микробиоте групп, формирующих провоспалительный (Bacteroides, Ruminococcus gnavus) или противовоспалительный (Faecalibacterium prausnitzii, Roseburia inulinivorans) фон. Первых гораздо чаще находили у лиц с бедным метагеномом.
Результаты проекта MetaHIT однозначно говорят о том, что обилие кишечной микрофлоры человека коррелирует с его метаболическими маркерами, при этом гены бактерий играют чуть ли не бóльшую роль в патогенезе ожирения, чем наши собственные.
Среди обладателей «малого генома» (23% от всех участников) было больше людей с избыточным весом. Для этой группы в целом были характерны нарушения в ответе тканей на действие инсулина, что вело к повышению его концентрации в крови. У таких людей выявлялось и статистически достоверное снижение содержания так называемого «хорошего холестерина» — липопротеинов высокой плотности, переносящих холестерин от различных тканей к печени для дальнейшей трансформации и утилизации. Также отмечалась тенденция к повышению в крови уровня триглицеридов, свободных жирных кислот и гормона лептина, высокие концентрации которого рассматриваются как независимый фактор риска развития сердечно-сосудистых патологий и тромбозов. (К основным факторам риска относят также специфические варианты липидного профиля, высокое артериальное давление, хронический воспалительный фон и курение.)
В ряде исследований показано, что у людей, в рационе которых преобладают растительные компоненты, в микробиоме доминируют бактерии, расщепляющие полисахариды, — а это как раз представители типа Bacteroidetes, часть которых защищает хозяина от развития локального и системного воспаления. В то же время у любителей растительной пищи снижается количество фирмикутов, а также энтеробактерий, которых нередко называют «патобионтами»: они способны создавать воспалительную среду благодаря липополисахариду своей внешней мембраны и повышению проницаемости кишечного эпителия, что ведет к масштабному проникновению молекул липополисахарида в кровоток и провокации метаболической эндотоксемии, а возможно, и тяги к регулярному перееданию. Кстати, именно так развиваются события на фоне высокожировой диеты. Вегетарианский же рацион, напротив, большинство исследований связывает со сниженным риском развития метаболического синдрома и связанных с ним «болезней цивилизации» [7].
Активное разложение растительной клетчатки соответствующими бактериями толстого кишечника ведет к образованию моносахаридов и короткоцепочечных жирных кислот (КЖК). Последние — особенно масляная кислота — необходимы не только кишечной микрофлоре, но и макроорганизму. Например, они снижают рН кишечного содержимого, вытесняя тем самым из сообщества ряд патобионтов, а главное — обеспечивают энергией энтероциты, защищают их от онкотрансформации и подавляют воспалительные сигнальные пути. Но и здесь не всё так однозначно: с одной стороны, избыток КЖК может усиливать липогенез и потому способствовать развитию ожирения, с другой — в некоторых работах показано благоприятное влияние КЖК на липидный профиль и уровень глюкозы крови. Это позитивное влияние может быть опосредовано связыванием КЖК с клеточными рецепторами, сопряженными с G-белком, — GPR41 и GPR43, — что влечет за собой гормональные изменения, приводящие к ощущению сытости и повышению чувствительности тканей к инсулину. В целом, на последствия продукции микрофлорой больших количеств КЖК влияет масса факторов — от типа и количества пищевого «сырья» до вариаций в бактериальном составе, заложенных еще на ранних этапах развития организма . С другой стороны, пищевые волокна предупреждают метаболические нарушения и независимо от состава микрофлоры. Более того, профилактический эффект преимущественно растительной диеты относительно развития атеросклероза показали исследования, связанные с биотрансформацией L-карнитина: именно некоторые кишечные бактерии, причем вполне полезные с других точек зрения, превращают содержащийся в красном мясе L-карнитин в атерогенные вещества [7], [12].
Захватывающую историю о заселении бактериями человеческого организма и ведущей роли колонизаторов в становлении «правильных» иммунных реакций хозяина рассказывает другая конкурсная статья: «Микробиом кишечника: мир внутри нас» [13]. — Ред.
Кишечные бактерии способны снижать уровень триглицеридов в крови, улучшать глюкозный и липидный метаболизм также за счет непосредственного участия в циркуляции желчных кислот, а уменьшать жировые запасы — путем активации уже упоминавшегося ингибитора липопротеинлипазы [10]. Но пока сложно делать какие-то выводы: слишком уж противоречивы иногда результаты экспериментов. Составить представление о противоречиях и их причинах, а главное — о возможных механизмах, связывающих деятельность микробиоты с метаболизмом хозяина, поможет новый обзор [10].
Лечение и профилактика СД 2-го типа тесно связаны с нормализацией веса. А она требует изменения характера питания (соотношения макро- и микронутриентов) в сочетании с увеличением физической активности: то есть важно создать условия некоторого энергетического дефицита, когда калорий тратится больше, чем поступает [14]. И хотя роль микробиоценоза кишечника в регуляции энергетического обмена ясна не до конца, уже сейчас понятно, что воздействие на микрофлору определенно может способствовать устранению ожирения и компенсации СД 2-го типа.
И, как ни странно, подобное воздействие способно переломить и тревожную ситуацию с заболеванием, в корне отличающимся патогенетически, — СД 1-го типа. Это аутоиммунное заболевание, связанное с агрессией Т-лимфоцитов против β-клеток поджелудочной железы, которые вырабатывают инсулин. Если в случае СД 2-го типа повышение уровня глюкозы в крови происходит вследствие нечувствительности тканей к инсулину (которая мешает клеткам усваивать глюкозу), то при СД 1-го типа просто не хватает самогό инсулина. Для развития этого заболевания требуется стечение ряда обстоятельств — генетических и средовых, а в числе последних, как оказалось, огромную роль играют перестройки кишечного микробиома. Нормофлора кишечника сразу после заселения тренирует иммунную систему хозяина, чтобы та различала своих и чужих, бурно реагировала на чужих, но вовремя останавливалась [13]. Видимо, при СД 1-го типа что-то в этой цепочке ломается.
В одном из экспериментов с крысами, предрасположенными к СД 1-го типа, выявили различия в составе кишечной микрофлоры у животных с уже развившимся диабетом и без него [15]. У последних обнаружили более низкое содержание, как ни странно, представителей типа Bacteroidetes — того, что в ряде исследований от метаболических расстройств, скорее, защищал. Но, как мы знаем, эффекты бактерий радикально разнятся не то что от типа к типу, а даже от штамма к штамму. Применение антибиотиков у этих крыс предотвращало развитие диабета. Исследователи предположили, что изменения кишечной микрофлоры, вызванные приемом антибиотиков, приводят к снижению общей антигенной нагрузки и последующего воспаления, которое может способствовать разрушению β-клеток поджелудочной железы. Однако, как водится, в ряде других экспериментов с животными и людьми эффект антибиотиков (которые, конечно, различались) был обратным [16].
У человеческих детей с СД 1-го типа и здоровых контролей выявили существенную разницу в составе кишечной микробиоты, причем у диабетиков было повышено соотношение Bacteroidetes/Firmicutes и преобладали бактерии, утилизирующие молочную кислоту. У здоровых детей было больше продуцентов масляной кислоты. В целом полагают, что определенные отклонения в составе микрофлоры, происходящие преимущественно в критические периоды онтогенеза (во время эмбриогенеза, рождения, грудного вскармливания и пубертата) способствуют усилению провоспалительной сигнализации со всеми вытекающими иммунными последствиями [16]. Возможно, что из-за сопутствующего нарушения барьерной функции кишечного эпителия выходящие в кровоток и проникающие в панкреатические лимфоузлы бактериальные антигены взаимодействуют с рецепторами NOD2 и провоцируют Т-клетки на атаку панкреатических β-клеток [17].
Таким образом, полученные к настоящему моменту данные создают основу для дальнейшего изучения роли кишечной микрофлоры в механизмах развития ожирения и сахарного диабета 1-го и 2-го типов, а также указывают на возможность профилактики и лечения этих патологий новыми способами — с помощью коррекции нашего микробиома.
источник
Микрофлора кишечника человека является составляющей человеческого организма и выполняет многочисленные жизненно важные функции. Общая численность микроорганизмов, обитающих в различных частях макроорганизма, приблизительно на два порядка превышает числен
Микрофлора кишечника человека является составляющей человеческого организма и выполняет многочисленные жизненно важные функции. Общая численность микроорганизмов, обитающих в различных частях макроорганизма, приблизительно на два порядка превышает численность его собственных клеток и составляет около 10 14–15 . Совокупный вес микроорганизмов человеческого тела составляет около 3–4 кг. Наибольшее число микроорганизмов приходится на желудочно-кишечный тракт (ЖКТ), включая ротоглотку (75–78%), остальные заселяют мочеполовые пути (до 2–3% у мужчин и до 9–12% у женщин) и кожные покровы.
У здоровых лиц в кишечнике насчитывается более 500 видов микроорганизмов. Общая масса микрофлоры кишечника составляет от 1 до 3 кг. В разных отделах ЖКТ количество бактерий различно, большинство микроорганизмов локализованы в толстой кишке (около 10 10–12 КОЕ/мл, что составляет 35–50% ее содержимого). Состав кишечной микрофлоры достаточно индивидуален и формируется с первых дней жизни ребенка, приближаясь к показателям взрослого к концу 1-го — 2-му году жизни, претерпевая некоторые изменения в пожилом возрасте (табл. 1). У здоровых детей в толстой кишке обитают представители факультативно-анаэробных бактерий рода Streptococcus, taphylococcus, Lactobacillus, nterobacteriacae, Candida и более чем 80% биоценоза занимают анаэробные бактерии, чаще грамположительные: пропионобактерии, вейлонеллы, эубактерии, анаэробные лактобациллы, пептококки, пептострептококки, а также грамотрицательные бактероиды и фузобактерии.
Распределение микроорганизмов по ходу ЖКТ имеет достаточно строгие закономерности и тесно коррелирует с состоянием пищеварительной системы (табл. 2). Большинство микроорганизмов (около 90%) присутствуют в тех или иных отделах постоянно и являются основной (резидентной) микрофлорой; около 10% составляет факультативная (или добавочная, сопутствующая микрофлора); и 0,01–0,02% приходится на долю случайных (или транзиторных, остаточных) микроорганизмов. Условно принято считать, что главная микрофлора толстой кишки представлена анаэробными бактериями, тогда как аэробные бактерии составляют сопутствующую микрофлору. Стафилококки, клостридии, протей и грибы относятся к остаточной микрофлоре. Помимо этого, в толстой кишке выявляются около 10 кишечных вирусов и некоторые представители непатогенных простейших. Облигатных и факультативных анаэробов в толстой кишке всегда на порядок больше, чем аэробов, причем строгие анаэробы непосредственно адгезированы на эпителиоцитах, выше располагаются факультативные анаэробы, далее — аэробные микроорганизмы. Таким образом, анаэробные бактерии (в основном бифидобактерии и бактероиды, суммарная доля которых составляет около 60% от общего количества анаэробных бактерий) являются наиболее постоянной и многочисленной группой микрофлоры кишечника, осуществляющей основные функции.
Вся совокупность микроорганизмов и макроорганизм составляют своеобразный симбиоз, где каждый извлекает выгоды для своего существования и оказывает влияние на партнера. Функции кишечной микрофлоры по отношению к макроорганизму реализуются как локально, так и на системном уровне, при этом различные виды бактерий вносят свой вклад в это влияние. Микрофлора пищеварительного тракта выполняет следующие функции.
- Морфокинетические и энергетические эффекты (энергообеспечение эпителия, регулирование перистальтики кишечника, тепловое обеспечение организма, регуляция дифференцировки и регенерации эпителиальных тканей).
- Формирование защитного барьера слизистой оболочки кишечника, подавление роста патогенной микрофлоры.
- Иммуногенная роль (стимуляция иммунной системы, стимуляция местного иммунитета, в том числе выработки иммуноглобулинов).
- Модуляция функций цитохромов Р450 в печени и продукция Р450-схожих цитохромов.
- Детоксикация экзогенных и эндогенных токсических субстанций и соединений.
- Продукция разнообразных биологически активных соединений, активация некоторых лекарственных препаратов.
- Мутагенная/антимутагенная активность (повышение резистентности эпителиальных клеток к мутагенам (канцерогенам), разрушение мутагенов).
- Регуляция газового состава полостей.
- Регуляция поведенческих реакций.
- Регуляция репликации и экспрессии генов прокариотических и эукариотических клеток.
- Регуляция запрограммированной гибели эукариотических клеток (апоптоза).
- Хранилище микробного генетического материала.
- Участие в этиопатогенезе заболеваний.
- Участие в водно-солевом обмене, поддержание ионного гомеостаза организма.
- Формирование иммунологической толерантности к пищевым и микробным антигенам.
- Участие в колонизационной резистентности.
- Обеспечение гомеостаза симбиотических взаимоотношений прокариотических и эукариотических клеток.
- Участие в обмене веществ: метаболизме белков, жиров (поставка субстратов липогенеза) и углеводов (поставка субстратов глюконеогенеза), регуляция желчных кислот, стероидов и др. макромолекул.
Так, бифидобактерии за счет ферментации олиго- и полисахаридов продуцируют молочную кислоту и ацетат, которые обеспечивают бактерицидную среду, секретируют вещества-ингибиторы роста патогенных бактерий, что повышает резистентность организма ребенка к кишечным инфекциям. Модуляции иммунного ответа ребенка бифидобактериями также выражаются в снижении риска развития пищевой аллергии.
Лактобациллы уменьшают активность пероксидазы, оказывая антиоксидантный эффект, обладают противоопухолевой активностью, стимулируют продукцию иммуноглобулина А (IgA), подавляют рост патогенной микрофлоры и стимулируют рост лакто- и бифидофлоры, оказывают противовирусное действие.
Из представителей энтеробактерий наиболее важное значение имеет Escherichia coli M17, которая вырабатывает колицин В, за счет чего подавляет рост шигелл, сальмонелл, клебсиелл, серраций, энтеробактеров и оказывает незначительное влияние на рост стафилококков и грибов. Также кишечная палочка способствуют нормализации микрофлоры после антибактериальной терапии и воспалительных и инфекционных заболеваний.
Энтерококки (Enterococcus avium, faecalis, faecium) стимулируют местный иммунитет за счет активации В-лимфоцитов и повышения синтеза IgA, высвобождения интерлейкинов-1β и -6, γ-интерферона; обладают противоаллергическим и антимикотическим действием.
Кишечные палочки, бифидо- и лактобактерии выполняют витаминообразующую функцию (участвуют в синтезе и всасывании витаминов К, группы В, фолиевой и никотиновой кислот). По способности синтезировать витамины кишечная палочка превосходит все остальные бактерии кишечной микрофлоры, синтезируя тиамин, рибофлавин, никотиновую и пантотеновую кислоты, пиридоксин, биотин, фолиевую кислоту, цианокобаламин и витамин К. Бифидобактерии синтезируют аскорбиновую кислоту, бифидо- и лактобактерии способствуют всасыванию кальция, витамина D, улучшают всасывание железа (благодаря созданию кислой среды).
Процесс пищеварения условно можно разделить на собственное (дистанционное, полостное, аутолитическое и мембранное), осуществляемое ферментами организма, и симбиозное пищеварение, происходящее при содействии микрофлоры. Микрофлора кишечника человека участвует в ферментации нерасщепленных ранее компонентов пищи, главным образом углеводов, таких, как крахмал, олиго- и полисахариды (в том числе и целлюлоза), а также белков и жиров.
Не всосавшиеся в тонкой кишке белки и углеводы в слепой кишке подвергаются более глубокому бактериальному расщеплению — преимущественно кишечной палочкой и анаэробами. Конечные продукты, образующиеся в результате процесса бактериальной ферментации, оказывают различное влияние на состояние здоровья человека. Например, бутират необходим для нормального существования и функционирования колоноцитов, является важным регулятором их пролиферации и дифференцировки, а также всасывания воды, натрия, хлора, кальция и магния. Вместе с другими летучими жирными кислотами он оказывает влияние на моторику толстой кишки, в одних случаях ускоряя ее, в других — замедляя. При расщеплении полисахаридов и гликопротеинов внеклеточными микробными гликозидазами образуются, помимо прочего, моносахариды (глюкоза, галактоза и т. д.), при окислении которых в окружающую среду выделяется в виде тепла не менее 60% их свободной энергии.
Среди важнейших системных функций микрофлоры — поставка субстратов глюконеогенеза, липогенеза, а также участие в метаболизме белков и рециркуляции желчных кислот, стероидов и других макромолекул. Превращение холестерина в не всасывающийся в толстой кишке копростанол и трансформация билирубина в стеркобилин и уробилин возможны только при участии бактерий, находящихся в кишечнике.
Протективная роль сапрофитной флоры реализуется как на местном, так и на системном уровнях. Создавая кислую среду, благодаря образованию органических кислот и снижению рН среды толстой кишки до 5,3–5,8, симбионтная микрофлора защищает человека от колонизации экзогенными патогенными микроорганизмами и подавляет рост уже имеющихся в кишечнике патогенных, гнилостных и газообразующих микроорганизмов. Механизм этого явления заключается в конкуренции микрофлоры за питательные вещества и участки связывания, а также в выработке нормальной микрофлорой определенных ингибирующих рост патогенов субстанций, обладающих бактерицидной и бактериостатической активностью, в том числе антибиотикоподобных. Низкомолекулярные метаболиты сахаролитической микрофлоры, в первую очередь летучие жирные кислоты, лактат и др., обладают заметным бактериостатическим эффектом. Они способны ингибировать рост сальмонелл, дизентерийных шигелл, многих грибов.
Также кишечная микрофлора усиливает местный кишечный иммунологический барьер. Известно, что у стерильных животных в lamina propria определяется очень малое количество лимфоцитов, кроме того, у этих животных наблюдается иммунодефицит. Восстановление нормальной микрофлоры быстро приводит к увеличению количества лимфоцитов в слизистой кишечника и исчезновению иммунодефицита. Сапрофитные бактерии в определенной степени обладают способностью модулировать уровень фагоцитарной активности, снижая его у людей, страдающих аллергией и, наоборот, повышая его у здоровых индивидуумов.
Таким образом, микрофлора ЖКТ не только формирует местный иммунитет, но и играет огромную роль в становлении и развитии иммунной системы ребенка, а также поддерживает ее активность у взрослого. Резидентная флора, особенно некоторые микроорганизмы, обладают достаточно высокими иммуногенными свойствами, что стимулирует развитие лимфоидного аппарата кишечника и местный иммунитет (в первую очередь за счет усиления продукции ключевого звена системы местного иммунитета — секреторного IgA), а также приводит к системному повышению тонуса иммунной системы, с активацией клеточного и гуморального звеньев иммунитета. Системная стимуляция иммунитета — одна из важнейших функций микрофлоры. Известно, что у безмикробных лабораторных животных не только подавлен иммунитет, но и происходит инволюция иммунокомпетентных органов. Поэтому при нарушениях микроэкологии кишечника, дефиците бифидофлоры и лактобацилл, беспрепятственном бактериальном заселении тонкой и толстой кишки возникают условия для снижения не только местной защиты, но и резистентности организма в целом.
Несмотря на достаточную иммуногенность, сапрофитные микроорганизмы не вызывают реакций иммунной системы. Возможно, это происходит потому, что сапрофитная микрофлора является своего рода хранилищем микробных плазмидных и хромосомных генов, обмениваясь генетическим материалом с клетками хозяина. Реализуются внутриклеточные взаимодействия путем эндоцитоза, фагоцитоза и пр. При внутриклеточных взаимодействиях достигается эффект обмена клеточным материалом. В результате представители микрофлоры приобретают рецепторы и другие антигены, присущие хозяину. Это делает их «своими» для иммунной системы макроорганизма. Эпителиальные ткани в результате такого обмена приобретают бактериальные антигены.
Обсуждается вопрос о ключевом участии микрофлоры в обеспечении противовирусной защиты хозяина. Благодаря феномену молекулярной мимикрии и наличию рецепторов, приобретенных от эпителия хозяина, микрофлора становится способной к перехвату и выведению вирусов, обладающих соответствующими лигандами.
Таким образом, наряду с низким рН желудочного сока, двигательной и секреторной активностью тонкой кишки, микрофлора ЖКТ относится к неспецифическим факторам защиты организма.
Важной функцией микрофлоры является синтез ряда витаминов. Человеческий организм получает витамины в основном извне — с пищей растительного или животного происхождения. Поступающие витамины в норме всасываются в тонкой кишке и частично утилизируются кишечной микрофлорой. Микроорганизмы, населяющие кишечник человека и животных, продуцируют и утилизируют многие витамины. Примечательно, что наиболее важную роль для человека в этих процессах играют микробы тонкой кишки, так как продуцируемые ими витамины могут эффективно всасываться и поступать в кровоток, тогда как витамины, синтезирующиеся в толстой кишке, практически не всасываются и для человека оказываются недоступными. Подавление микрофлоры (например, антибиотиками) снижает и синтез витаминов. Наоборот, создание благоприятных для микроорганизмов условий, например при употреблении в пищу достаточного количества пребиотиков, повышает обеспеченность макроорганизма витаминами.
Наиболее изучены в настоящее время аспекты, связанные с синтезом кишечной микрофлорой фолиевой кислоты, витамина В12 и витамина К.
Фолиевая кислота (витамин В9), поступая с продуктами питания, эффективно всасывается в тонкой кишке. Синтезирующийся в толстой кишке представителями нормальной кишечной микрофлоры фолат идет исключительно для ее собственных нужд и не утилизируется макроорганизмом. Тем не менее синтез фолата в толстой кишке может иметь большое значение для нормального состояния ДНК колоноцитов.
Кишечные микроорганизмы, синтезирующие витамин В12, обитают как в толстой, так и в тонкой кишке. Среди этих микроорганизмов наиболее активны в данном аспекте представители Pseudomonas и Klebsiella sp. Однако возможностей микрофлоры для полной компенсации гиповитаминоза В12 оказывается недостаточно.
С содержанием в просвете толстой кишки фолата и кобаламина, полученных с пищей или синтезированных микрофлорой, связана способность эпителия кишечника противостоять процессам канцерогенеза. Предполагается, что одной из причин более высокой частоты опухолей толстой кишки, по сравнению с тонкой, является недостаток цитопротекторных составляющих, большинство из которых всасывается в средних отделах ЖКТ. Среди них — витамин В12 и фолиевая кислота, которые совместно определяют стабильность клеточных ДНК, в частности ДНК клеток эпителия толстой кишки. Даже незначительный дефицит этих витаминов, не вызывающий анемию или другие тяжелые последствия, тем не менее приводит к значимым аберрациям в молекулах ДНК колоноцитов, способным стать основой канцерогенеза. Известно, что недостаточное поступление к колоноцитам витаминов В6, В12 и фолиевой кислоты ассоциируется с повышенной частотой рака толстой кишки в популяции. Дефицит витаминов приводит к нарушению процессов метилирования ДНК, мутациям и, как следствие, раку толстой кишки. Риск толстокишечного канцерогенеза повышается при низком потреблении пищевых волокон и овощей, обеспечивающих нормальное функционирование кишечной микрофлоры, синтезирующей трофические и протективные в отношении толстой кишки факторы.
Витамин К существует в нескольких разновидностях и необходим человеческому организму для синтеза различных кальцийсвязывающих белков. Источником витамина К1, филохинона, являются продукты растительного происхождения, а витамин К2, группа соединений менахинонов, синтезируется в тонкой кишке человека. Микробный синтез витамина К2 стимулируется при недостатке филохинона в диете и вполне способен его компенсировать. В то же время недостаточность витамина К2 при сниженной активности микрофлоры плохо корригируется диетическими мероприятиями. Таким образом, синтетические процессы в кишечнике являются приоритетными для обеспечения макроорганизма этим витамином. Витамин К синтезируется и в толстой кишке, но используется преимущественно для потребностей микрофлоры и колоноцитов.
Кишечная микрофлора принимает участие в детоксикации экзогенных и эндогенных субстратов и метаболитов (аминов, меркаптанов, фенолов, мутагенных стероидов и др.) и, с одной стороны, представляет собой массивный сорбент, выводя из организма токсические продукты с кишечным содержимым, а с другой — утилизирует их в реакциях метаболизма для своих нужд. Помимо этого, представители сапрофитной микрофлоры продуцируют на основе конъюгатов желчных кислот эстрагеноподобные субстанции, оказывающие влияние на дифференцировку и пролиферацию эпителиальных и некоторых других тканей путем изменения экспрессии генов или характера их действия.
Итак, взаимоотношения микро- и макроорганизма носят сложный характер, реализующийся на метаболическом, регуляторном, внутриклеточном и генетическом уровне. Однако нормальное функционирование микрофлоры возможно только при хорошем физиологическом состоянии организма и в первую очередь нормальном питании.
Питание микроорганизмов, населяющих кишечник, обеспечивается за счет нутриентов, поступающих из вышележащих отделов ЖКТ, которые не перевариваются собственными ферментативными системами и не всасываются в тонкой кишке. Эти вещества необходимы для обеспечения энергетических и пластических потребностей микроорганизмов. Способность использовать нутриенты для своей жизнедеятельности зависит от ферментативных систем различных бактерий.
В зависимости от этого условно выделяют бактерии с преимущественно сахаролитической активностью, основным энергетическим субстратом которых являются углеводы (характерно в основном для сапрофитной флоры), с преимущественной протеолитической активностью, использующих белки для энергетических целей (характерно для большинства представителей патогенной и условно-патогенной флоры), и смешанной активностью. Соответственно, преобладание в пище тех или иных нутриентов, нарушение их переваривания будет стимулировать рост различных микроорганизмов.
Углеводные нутриенты особенно необходимы для жизнедеятельности нормальной кишечной микрофлоры. Ранее эти компоненты пищи называли «балластными», предполагая, что они не имеют какого-либо существенного значения для макроорганизма, однако по мере изучения микробного метаболизма стало очевидно их значение не только для роста кишечной микрофлоры, но для здоровья человека в целом. Согласно современному определению, пребиотиками называют частично или полностью не перевариваемые компоненты пищи, которые избирательно стимулируют рост и/или метаболизм одной или нескольких групп микроорганизмов, обитающих в толстой кишке, обеспечивая нормальный состав кишечного микробиоценоза. Свои энергетические потребности микроорганизмы толстой кишки обеспечивают за счет анаэробного субстратного фосфорилирования, ключевым метаболитом которого является пировиноградная кислота (ПВК). ПВК образуется из глюкозы в процессе гликолиза. Далее, в результате восстановления ПВК, образуется от одной до четырех молекул аденозинтрифосфата (АТФ). Последний этап приведенных выше процессов обозначается как брожение, которое может идти различными путями с образованием различных метаболитов.
Гомоферментативное молочное брожение характеризуется преимущественным образованием молочной кислоты (до 90%) и характерно для лактобактерий и стрептококков толстой кишки. Гетероферментативное молочное брожение, при котором образуются и другие метаболиты (в том числе уксусная кислота), присуще бифидобактериям. Спиртовое брожение, ведущее к образованию углекислого газа и этанола, является побочным метаболическим эффектом у некоторых представителей Lactobacillus и Clostridium. Отдельные виды энтеробактерий (E. coli) и клостридий получают энергию в результате муравьинокислого, пропионового, маслянокислого, ацетонобутилового или гомоацетатного видов брожения.
В результате микробного метаболизма в толстой кишке образуются молочная кислота, короткоцепочечные жирные кислоты (С2 — уксусная; С3 — пропионовая; С4 — масляная/изомасляная; С5 — валериановая/изовалериановая; С6 — капроновая/изокапроновая), углекислый газ, водород, вода. Углекислый газ в большой степени преобразуется в ацетат, водород всасывается и выводится через легкие, а органические кислоты (в первую очередь жирные короткоцепочечные) утилизируются макроорганизмом. Нормальная микрофлора толстой кишки, перерабатывая не переваренные в тонкой кишке углеводы, производит короткоцепочечные жирные кислоты с минимальным количеством их изоформ. В то же время при нарушении микробиоценоза и увеличении доли протеолитической микрофлоры указанные жирные кислоты начинают синтезироваться из белков преимущественно в виде изоформ, что отрицательно сказывается на состоянии толстой кишки, с одной стороны, и может быть диагностическим маркером — с другой.
Помимо этого, различные представители сапрофитной флоры имеют свои потребности в определенных нутриентах, объясняющиеся особенностями их метаболизма. Так, бифидобактерии расщепляют моно-, ди-, олиго- и полисахариды, используя их как энергетический и пластический субстрат. При этом они могут ферментировать белки, в том числе и для энергетических целей; не требовательны к поступлению с пищей большинства витаминов, но нуждаются в пантотенатах.
Лактобактерии также используют различные углеводы для энергетических и пластических целей, однако плохо расщепляют белки и жиры, поэтому нуждаются в поступлении извне аминокислот, жирных кислот, а также витаминов.
Энтеробактерии расщепляют углеводы с образованием углекислого газа, водорода и органических кислот. При этом существуют лактозонегативные и лактозопозитивные штаммы. Также они могут утилизировать белки и жиры, поэтому мало нуждаются во внешнем поступлении аминокислот, жирных кислот и большинства витаминов.
Очевидно, что питание сапрофитной микрофлоры и ее нормальное функционирование принципиально зависит от поступления к ней не переваренных углеводов (ди-, олиго- и полисахаридов) для энергетических целей, а также белков, аминокислот, пуринов и пиримидинов, жиров, углеводов, витаминов и минералов — для пластического обмена. Залогом поступления к бактериям необходимых нутриентов является рациональное питание макроорганизма и нормальное течение пищеварительных процессов.
Хотя моносахариды могут легко утилизироваться микроорганизмами толстой кишки, к пребиотикам их не относят.
В нормальных условиях кишечная микрофлора не потребляет моносахариды, которые должны полностью всасываться в тонкой кишке. Пребиотики включают некоторые дисахариды, олигосахариды, полисахариды и достаточно гетерогенную группу соединений, в которой присутствуют и поли- и олигосахариды, которую обозначили как пищевые волокна. Из пребиотиков в женском молоке присутствует лактоза и олигосахариды.
Лактоза (молочный сахар) представляет собой дисахарид, состоящий из галактозы и глюкозы. В норме лактоза расщепляется лактазой тонкой кишки до мономеров, которые практически полностью всасываются в тонкой кишке. Лишь незначительное количество нерасщепленной лактозы у детей первых месяцев жизни попадает в толстую кишку, где утилизируется микрофлорой, обеспечивая ее становление. В то же время дефицит лактазы приводит к избытку лактозы в толстой кишке и значительному нарушению состава кишечной микрофлоры и осмотической диарее.
Лактулоза — дисахарид, состоящий из галактозы и фруктозы, в молоке (женском или коровьем) отсутствует, однако в небольших количествах может образовываться при нагревании молока до температуры кипения. Лактулоза не переваривается ферментами ЖКТ, ферментируется лакто- и бифидобактериями и служит им субстратом для энергетического и пластического обмена, за счет чего способствует их росту и нормализации состава микрофлоры, увеличению объема биомассы в содержимом кишечника, что определяет ее слабительный эффект. Помимо этого, показана антикандидозная активность лактулозы и ее угнетающий эффект на сальмонелл. Полученная синтетическим путем лактулоза (дюфалак) широко используется как эффективное слабительное средство, обладающее пребиотическими свойствами. Как пребиотик детям дюфалак назначается в низких дозах, не оказывающих слабительного эффекта (по 1,5–2,5 мл 2 раза в день в течение 3–6 нед).
Олигосахариды представляют собой линейные полимеры глюкозы и других моносахаров с общей длиной цепи не более 10. По химической структуре выделяют галакто-, фрукто-, фукозил-олигосахариды и др. Концентрация олигосахаридов в женском молоке относительно невелика, не более 12–14 г/л, однако их пребиотический эффект весьма значителен. Именно олигосахариды сегодня рассматриваются как основные пребиотики женского молока, обеспечивающие как становление нормальной микрофлоры кишечника ребенка, так и ее поддержание в дальнейшем. Важным является то обстоятельство, что олигосахариды присутствуют в значимых концентрациях только в женском молоке и отсутствуют, в частности, в коровьем. Следовательно, в состав адаптированных молочных смесей для искусственного вскармливания здоровых детей должны добавляться пребиотики (галакто- и фруктосахариды).
Полисахариды представляют собой длинноцепочечные углеводы в основном растительного происхождения. Инулин, содержащий фруктозу, в больших количествах присутствует в артишоках, клубнях и корнях георгинов и одуванчиков; утилизируется бифидо- и лактобактериями, способствует их росту. Помимо этого, инулин повышает всасывание кальция и влияет на метаболизм липидов, снижая риск развития атеросклероза.
Пищевые волокна — большая гетерогенная группа полисахаридов, наиболее известными из которых являются целлюлоза и гемицеллюлоза. Целлюлоза — неразветвленный полимер глюкозы, а гемицеллюлоза — полимер глюкозы, арабинозы, глюкуроновой кислоты и ее метилового эфира. Помимо функции субстрата для питания лакто- и бифидофлоры и опосредованно поставщика короткоцепочечных жирных кислот для колоноцитов, пищевые волокна оказывают и другие важные эффекты. Они обладают высокой адсорбционной способностью и удерживают воду, что приводит к повышению осмотического давления в полости кишки, увеличению объема фекалий, ускорения пассажа по кишечнику, что обусловливает слабительный эффект.
В средних количествах (1–1,9 г/100 г продукта) пищевые волокна содержатся в моркови, сладком перце, петрушке (в корне и зелени), редьке, репе, тыкве, дыне, черносливе, цитрусовых, бруснике, фасоли, гречневой, перловой крупе, «Геркулесе», ржаном хлебе.
Высокое содержание (2–3 г/100 г продукта) пищевых волокон характерно для чеснока, клюквы, красной и черной смородины, черноплодной рябины, ежевики, овсяной крупы, хлеба из белково-отрубной муки.
Наибольшее же их количество (более 3 г/100 г) содержится в укропе, кураге, клубнике, малине, чае (4,5 г/100 г), овсяной муке (7,7 г/100 г), пшеничных отрубях (8,2 г/100 г), сушеном шиповнике (10 г/100 г), жареном кофе в зернах (12,8 г/100 г), овсяных отрубях (14 г/100 г). Пищевые волокна отсутствуют в рафинированных продуктах.
Несмотря на очевидную значимость пребиотиков для питания микрофлоры, благополучия ЖКТ и всего организма в целом, в современных условиях отмечается дефицит пребиотиков в питании во всех возрастных группах. В частности, взрослый человек должен съедать в сутки примерно 20–35 г пищевых волокон, тогда как в реальных условиях европеец потребляет не более 13 г в сутки. Уменьшение доли естественного вскармливания у детей первого года жизни приводит к недостатку пребиотиков, содержащихся в женском молоке.
Таким образом, пребиотики обеспечивают благополучие микрофлоры толстой кишки, здоровье толстой кишки и являются необходимым фактором здоровья человека в связи с их существенными метаболическими эффектами. Преодоление дефицита пребиотиков в современных условиях связано с обеспечением рационального питания лиц всех возрастных категорий, начиная от новорожденных и кончая людьми преклонного возраста.
- Ардатская М. Д., Минушкин О. Н., Иконников Н. С. Дисбактериоз кишечника: понятие, диагностические подходы и пути коррекции. Возможности и преимущества биохимического исследования кала: пособие для врачей. М., 2004. 57 с.
- Бельмер С. В., Гасилина Т. В. Рациональное питание и состав кишечной микрофлоры//Вопросы детской диетологии. 2003. Т. 1. № 5. С. 17–20.
- Доронин А. Ф., Шендеров Б. А. Функциональное питание. М.: ГРАНТЪ, 2002. 296 с.
- Конь И. Я. Углеводы: новые взгляды на их физиологические функции и роль в питании//Вопросы детской диетологии. 2005. Т. 3. № 1. С. 18–25.
- Boehm G., Fanaro S., Jelinek J., Stahl B., Marini A. Prebiotic concept for infant nutrition//Acta Paediatr Suppl. 2003; 91: 441: 64–67.
- Choi S. W., Friso S., Ghandour H., Bagley P. J., Selhub J., Mason J. B. Vitamin B12 deficiency induces anomalies of base substitution and methylation in the DNA of rat colonic epithelium//J. Nutr. 2004; 134 (4): 750–755.
- Edwards C. A., Parrett A. M. Intestinal flora during the first months of life: new perspectives//Br. J. Nutr. 2002; 1: 11–18.
- Fanaro S., Chierici R., Guerrini P., Vigi V. Intestinal microflora in early infancy: composition and development //Acta Paediatr. 2003; 91: 48–55.
- Hill M. J. Intestinal flora and endogenous vitamin synthesis//Eur. J. Cancer. Prev. 1997; 1: 43–45.
- Midtvedt A. C., Midtvedt T. Production of short chain fatty acids by the intestinal microflora during the first 2 years of human life//J. Pediatr. Gastroenterol. Nutr. 1992; 15: 4: 395–403.
С. В. Бельмер, доктор медицинских наук, профессор
А. В. Малкоч, кандидат медицинских наук
РГМУ, Москва
источник
Микрофлора кишечника – уникальная среда, которая не только принимает участие в пищеварении, а и способна вырабатывать целый ряд важных для жизни организма витаминов.
Каждый слышал, что для нормального функционирования организм нуждается в витаминах. Чтобы не навредить здоровью, перед покупкой аптечного препарата стоит знать, какой витамин синтезируется микрофлорой кишечника, и есть ли нужда в его дополнительном употреблении.
Интересно! Всего, на текущий момент известно 13 витаминов. Эти данные обновляются в результате постоянных научных исследований в области биохимии, фармакологии. Изучением витаминов и их влияния на организм занимается витаминология.
На данный момент известно, что микрофлора кишечника вырабатывает 5 различных по действию, необходимых для здоровья и жизнедеятельности организма витаминов:
- Ниацин (В3) – благодаря ему происходят окислительные и восстановительные процессы в организме, обеспечивается обновление клеток. Вещество укрепляет сосуды, контролирует работу сердечно-сосудистой, пищеварительной системы. Также регулирует артериальное давление, снижает уровень вредного холестерина, в целом очищает организм от токсинов. Его синтез возможен при нормальном поступлении в организм витаминов В2 и В6;
- Биотин (В7) – регулирует жировой, углеводный и белковый обмен. Необходим для нормального переваривания пищи и поддержания высокого уровня метаболизма. При нарушении его выработки, человек отмечает увеличение массы тела и другие проблемы;
- Фолиевая кислота (В9) – отвечает за формирование кровяных телец, нормальную деятельность головного мозга и нервной системы. Укрепляет иммунитет, участвует в образовании нервной системы и головного мозга плода, поэтому беременным особенно важно поддерживать здоровье микрофлоры кишечника, а также дополнительно принимать витамин;
- Цианокобаламин (В12) – необходим для переваривания жиров, белков и углеводов. Участвует в формировании и деятельности нервной системы, контролирует деление ДНК и РНК. Это водорастворимый элемент, и он не накапливается в организме;
- Витамин К – отвечает за свертываемость крови и продукцию костного белка. Его недостаток проявляется ломкостью сосудов, подкожными кровоизлияниями. При постоянном значительном дефиците могут появиться кровоизлияния внутренних органов. В то же время переизбыток витамина К ведет к сильному сгущению крови и риску тромбоза.
Каждый из перечисленных витаминов синтезируется разными участками кишечника. Залогом их регулярной продукции является здоровая микрофлора, поэтому крайне важно поддерживать ее в норме.
Как правило, главной причиной нарушения баланса микрофлоры кишечника является сам человек, точнее его образ жизни. Но также нередко встречаются люди с врожденными патологиями внутренних органов, что становится причиной их неспособности полноценно функционировать.
Что касается приобретенных заболеваний, то чаще всего нарушает микрофлору дисбактериоз. Причинами его развития являются следующие:
- злоупотребление алкоголем, курение;
- длительный бесконтрольный прием антибиотических препаратов и различных ферментов;
- нерегулярное и скудное на ценные вещества питание, перекусы на ходу, «сухомятка», избыток сладких и жирных продуктов в рационе;
- нарушение режима сна и бодрствования. Известно, что во время сна организм восстанавливается. Если человек спит менее 7 часов на регулярной основе, это крайне негативно отражается на здоровье в целом и микрофлоре в частности;
- недостаток в питании белка, клетчатки;
- болезни эндокринной системы, гормональные сбои;
- частые психологические травмы, нервные переживания и стрессы;
- инфекционные, аллергические заболевания.
Также дисбактериоз развивается при недостаточной физической активности, злоупотреблении слабительными препаратами, увлечении голодными диетами.
Чтобы вернуть полноценность микрофлоры, необходимо устранить главную причину и обеспечить организм полезными микроорганизмами. Достигается это путем приема назначенных препаратов и сбалансированного питания.
Если имеются признаки интоксикации, врач назначит лекарства, которые очистят организм, выведут патогенную флору. Как правило, с этой целью прописываются антибактериальные средства на основе пенициллина, сорбенты. Далее назначаются препараты с высоким содержанием полезных микроорганизмов и пищевые биодобавки, содержащие пробиотики, пребиотики и симбиотики. К первым относятся те самые активные микроорганизмы, ко вторым – сопутствующие культуры и к третьим – комплекс микроорганизмов и субкультур.
Для устранения неприятных симптомов дисбактериоза назначаются средства против метеоризма, снимающие боли. Также показан прием лекарств, нормализующих моторику кишечника, с целью профилактики застойных явлений и повторных интоксикаций; ферментов, улучшающих пищеварение.
Важно! Каждому пациенту врач назначает индивидуальную программу по восстановлению микрофлоры кишечника. Самолечение небезопасно.
Помимо лекарств важно пересмотреть свой рацион и сбалансировать его. Для этого нужно приучить себя к режиму дня, регулярному питанию. Составить меню из цельных, полезных продуктов животного и растительного происхождения.
Чтобы поддерживать в норме перистальтику кишечника, необходимы регулярные физические нагрузки, прогулки на свежем воздухе, спорт, активный отдых.
По разным причинам, количества вырабатываемых организмом витаминов может быть недостаточно для жизнедеятельности. Особенно это касается лиц, активно занятых интеллектуальной и физической работой, регулярно занимающихся спортом. Даже если питание сбалансировано и видимых причин со здоровьем нет, стоит пополнять организм витаминами.Здоровому человеку обеспечить норму витаминов вполне реально качественным питанием. Но если, например, вы живете в северных регионах, и ваш рацион беден на фрукты и овощи, стоит подобрать аптечный комплекс.
источник
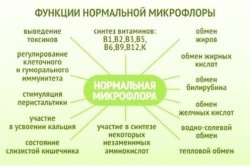
Микрофлора кишечника является чувствительной и сложной системой. Она состоит из бифидо- и лактобактерий, благодаря чему организм может самостоятельно бороться с болезнетворными вирусами и патогенными микробами. Здоровую функцию иммунной системы поддерживает также регулярный синтез собственных витаминов – этот процесс происходит преимущественно в нижних отделах кишечника.
- Витамин К. Необходим для выработки костного белка и полноценной свертываемости крови. При недостаточности витамина человек страдает от подкожных кровоизлияний, слабости сосудов, носовых кровотечений (недостаток развивается у пациентов с дисбактериозом и патологиями ЖКТ).
- Витамин В3. Контролирует окислительные процессы и регенерацию клеток, а также работу нервной системы. Влияет на пищеварение, состояние сердца и сосудов, регулирует уровень АД, очищает организм от продуктов распада и снижает показатели холестерина в крови. Синтез происходит при достаточном поступлении витаминов В2 и В6.
- Витамин В9 (фолиевая кислота). Участвует в формировании кровяных телец, укрепляет иммунитет, регулирует деятельность головного и костного мозга. Крайне необходим беременным женщинам, для правильного формирования головного мозга и нервной системы у плода.
- Витамин В12. Отвечает за метаболизм жиров, углеводов и белков, принимает участие в формировании и функционировании центральной нервной системы, контролирует синтез ДНК и РНК. Витамин является водорастворимым. Его недостатком страдают женщины во время беременности, люди с заболеваниями ЖКТ и злоупотребляющие алкоголем.
- Витамин H (биотин). Регулирует обмен белков и жиров. Участвует в выработке ферментов, влияющих на углеводный обмен, синтез нуклеотидов и коллагена. Опосредованно влияет на состояние кожи. Участвует в переносе углекислого газа.
- Витамин PP (никотиновая кислота). Принимает участие в метаболизме белков, жиров, пуринов. Влияет на уровень липидов в крови и артериальное давление. Обладает слабым антикоагулянтным действием (разжижает кровь).
- Витамин B6 (адермин). Влияет на работу пищеварительного тракта и состояние кожи. Нехватка адермина ведет к нарушению переваривания пищи, повышает риск развития анемии.
За синтез каждого витамина отвечают разные участки кишечника, но большинство продуцируется в толстом отделе кишки. Чем лучше сбалансирован рацион питания, тем большее количество витаминов синтезируется кишечной микрофлорой.

Так, витамины группы B, вырабатываются, преимущественно, в недостаточных количествах:
- В12 вырабатывается в малом объеме, которого не хватает для нормальной жизнедеятельности. Его запасы пополняются путем употребления телячьей печени, лосося, морепродуктов, мяса говядины и баранины.
- Витамином В3 насыщены орехи, все зеленые овощи, кукуруза, гречневая крупа, печень, бобы, яйца и помидоры.
- Фолиевой кислотой (В9) богаты злаковые, свежие фрукты и овощи, молоко, овсяная крупа, рыба, мясо и яйца.
А вот витамин К синтезируется в достаточных количествах, поэтому при отсутствии заболеваний ЖКТ и нормальном балансе микрофлоры пополнять его запасы нет необходимости.
Факторы, из-за которых общее состояние микрофлоры кишечника ухудшается, зачастую провоцируются самим человеком, но иногда баланс нарушается по причине острых и хронических заболеваний. Наиболее распространенными причинами развивающегося дисбактериоза считаются:
- злоупотребление антибактериальными препаратами – использование этой группы лекарств показано при многих инфекционных заболеваниях, однако их бесконтрольный и необоснованный прием приводит к уничтожению не только патогенных, но и полезных бактерий в кишечнике;
- вредные привычки – курение и злоупотребление спиртными напитками;
- перекусы на бегу, преимущественно сухой пищей – бутербродами, фастфудом, сладкой и углеводной пищей;
- отсутствие в рационе белка и растительной клетчатки – именно эти элементы составляют основу правильного пищеварения и роста полезной микрофлоры;
- гормональный сбой в организме, эндокринные нарушения;
- слишком частое очищение кишечника – в группу риска входят женщины, принимающие препараты для похудения на основе слабительных компонентов;
- инфекционные и аллергические заболевания.
В первую очередь, для восстановления полезной микрофлоры кишечника и устранения признаков дисбактериоза, необходимо выявить его причины. Для этого рекомендуется обратиться к гастроэнтерологу и, при острых показаниях, к инфекционисту.
Если патология вызвана размножением патогенных микробов, врач назначит антибактериальные препараты пенициллинового ряда или Метронидазол.
Также больному показан прием лекарств на основе культур активных микроорганизмов, пищевых добавок, сорбентов и прочих медикаментов:
- Пробиотики – это средства с активными бактериальными культурами, например, Линекс. Их назначают при дисбактериозе, развившемся на фоне приема антибиотиков.
- Пребиотики – препараты с содержанием питательных субстратов для увеличения полезной микрофлоры. Они улучшают функции кишечника и восстанавливают нормальный баланс – это Лактофильтрум, Лактусан, Прелакс.
- Синбиотики – это сочетание пробиотиков и пребиотиков в одном препарате. К ним относятся Энтерол, Биофлор, Максилак, Нарине.
- Средства от метеоризма, например, Эспумизан;
- Энтеросорбенты, выводящие из организма продукты распада и токсины – Энтеросгель, Смекта, Активированный уголь, Энтерол;
- Препараты для восстановления моторики желудка и кишечника – Имодиум, Дебридат;
- Гепатопротекторы и желчегонные – Карсил, Эссенциале, Аллохол, Гепабене;
- Ферменты для восстановления пищеварительной функции – Креон, Пензитал.
Какие препараты нужны конкретному пациенту – определит врач, исходя из клинических симптомов и результатов анализов (кал на копрограмму и дисбактериоз).
Основные правила диетического питания:
-
приемы пищи должны соответствовать режиму, то есть проводиться в одно и то же время;
- диета должна включать пищевые волокна;
- в меню обязательно включаются молочные продукты, обогащенные комплексом бифидо- и лактобактерий;
- меню разрабатывается по индивидуальной схеме, с учетом списка непереносимости каких-либо продуктов.
Пребиотики – это олиго- и полисахариды, содержащиеся в продуктах: овощах, фруктах, злаковых. Они не всасываются, а ферментируются в тканях кишечника, обеспечивая источник энергии для размножения полезных лакто- и бифидобактерий. Получить эти вещества можно, употребляя лук, чеснок, морковь, тыкву, кабачки, кашу из овсяной крупы.
Олигосахариды с фруктозой содержатся в яблоках, грушах, абрикосах, бананах, ягодах и гранатах. Полисахаридом инулином богаты цикорий, корень лопуха, чеснок.
Употребляя пребиотики, можно обеспечить питание полезным бактериям, уничтожить патогенную флору кишечника, повысить всасывание питательных веществ.
Пробиотики в большом количестве содержатся в молочных и кисломолочных продуктах: кефир, йогурты, кумыс, ацидофилин, Активия, Актимель. Их ежедневное употребление оказывает антагонистическое действие на патогенную флору, смещая баланс в сторону полезных бактерий. Также они подавляют продукцию серотонина, что предотвращает аллергические реакции.
Со списком разрешенных продуктов во время восстановления нормальной микрофлоры кишечника можно ознакомиться в таблице.
| Дисбактериоз на фоне диареи | Дисбактериоз на фоне запора | |
| Мучные, хлебные изделия | Сухой хлеб, сухари, печенье из несдобного теста (перед едой засохшая корочка снимается) | Бисквиты и хлеб из муки 2 сорта подсушенные, несдобное печенье |
| Суп, бульон | Обезжиренные мясные или рыбные супы с отварной крупой и перетертым мясом | На некрепком мясном, рыбном, овощном бульоне |
| Яйца | Не более 2 в сутки, сваренных всмятку или добавленных в суп | Не более 2 в сутки, в виде парового омлета |
| Закуски | Запрещены | Салаты из сырых овощей с растительным маслом или сметаной, ветчина нежирных сортов, вымоченная сельдь, заливное. |
| Рыба | Любая нежирных сортов, приготовленная в виде котлет и фрикаделек на пару | Нежирная, в запеченном или отварном виде, можно есть морепродукты |
| Молочные продукты | Творог нежирный, кефир, сметана, простокваша, сыр – после стихания воспаления | Молоко, ряженка, кефир, сливки, творог, сметана, сыр неострых сортов |
| Фрукты, десерты | Перетертые яблоки, кисели из груш, черемухи, айвы | Любые свежие ягоды и фрукты, можно в виде мармелада, варенья |
| Жиры | Немного сливочного масла | Сливочное, растительное масло |
| Напитки | Чай черный, зеленый, отвары смородины и черемухи, какао и кофе на воде | Отвар шиповника, соки из свежих фруктов, чай с молоком |
| Соусы | На основе сливочного масла, в дополнение к нежирным блюдам | С добавлением зелени, на мясных и рыбных бульонах, томатный, сметанный |
Восстановление нормального баланса микрофлоры, при соблюдении режима питания и приеме нужных препаратов, занимает 3-4 недели.
источник

 приемы пищи должны соответствовать режиму, то есть проводиться в одно и то же время;
приемы пищи должны соответствовать режиму, то есть проводиться в одно и то же время;