Автор текста – Анисимова Елена Сергеевна.
Авторские права защищены. Продавать текст нельзя.
Курсив не зубрить.
Замечания можно присылать по почте: exam_bch@mail.ru
https://vk.com/bch_5
Параграф учебника по биохимии 20.2
«Виды оксидоредуктаз».
см. п.3.
См. таблицу в файле «20.2 Таблица оксидоредуктазы».
Определение.
Оксидоредуктазы – это класс ферментов, которые катализируют окислительно-восстановительные реакции.
Основные группы (не только подклассы) оксидоредуктаз:
дегидрогеназы, оксидазы, оксигеназы,
редуктазы, цитохромы и антиокислительные ферменты.
Что такое окисление и восстановление.
Окисление – это отщепление электрона,
а восстановление – это присоединение электрона.
Окисление и восстановления всегда сопряжены, то есть связаны,
потому что если одно вещество теряет электрон
и при этом окисляется,
то другое вещество этот электрон приобретает
и при этом восстанавливается.
При восстановлении органических субстратов
электроны часто присоединяются в составе атомов водорода
(каждый из которых состоит из одного электрона и одного протона),
источником которых является НАДФН,
который получает атомы водорода в ПФП (п.35).
При окислении органических субстратов
электроны отщепляются обычно в составе атомов водорода,
которые переносятся на кофермент (НАД и др.) или кислород.
Присоединение атомов кислорода
тоже является окислением органического субстрата,
поскольку присоединившиеся атомы кислорода притягивают к себе электронную плотность тех атомов, в которым они присоединились.
1. Д Е Г И Д Р О Г Е Н А З Ы
катализируют реакции дегидрирования,
то есть отщепления атомов водорода (Н).
При этом водород
(2 атома водорода, состоящие из 2 протонов и 2 электронов)
отщепляется от органического субстрата (R)
и переносится на кофермент (на КоФ – НАД+, ФАД или НАДФ+).
Формулируя короче – дегидрогеназы переносят 2 атома водорода
от субстрата на кофермент.
Субстрат до отщепления от него пары атомов водорода
называется восстановленным субстратом
и обозначается так – RН2;
где Н – это атомы водорода, которые будут отщепляться,
а R – это остальные атомы молекулы субстрата.
Субстрат после отщепления от него пары атомов водорода
обозначается так – R
и называется окисленным.
Кофермент, получающий атомы водорода,
до их присоединения обозначается как КоФ,
а после присоединения двух Н обозначается как КоФН2.
Поскольку при отщеплении атомов водорода
вещество теряет вместе с водородом
входящие в состав водорода электроны,
а потеря электронов называется окислением,
то RН2 – более восстановленное вещество, чем R,
а КоФН2 – более восстановленное вещество, чем КоФ.
Поэтому RН2 называют восстановленным субстратом,
а R – окисленным субстратом.
КоФ2 называют восстановленным коферментом
(восстановленной формой кофермента),
а КоФ – окисленным коферментом
(окисленной формой кофермента).
Схема реакции, которая катализируется дегидрогеназами,
может быть представлена в таком виде:
Где RH2 – это восстановленный субстрат
(органический субстрат до отщепления водорода),
КоФ – окисленный кофермент
(кофермент до присоединения к нему отщепленного от субстрата водорода),
R – окисленный субстрат
(органический субстрат после отщепления от него водорода),
КоФН2 – восстановленный кофермент
(кофермент после присоединения к нему отщепленного от субстрата водорода).
Коферменты, которые участвуют в работе дегидрогеназ:
НАД+, ФАД и НАДФ+.
НАД+, ФАД и НАДФ+ – это обозначения окисленных форм коферментов,
а НАДН,Н+, ФАДН2 и НАДФН,Н+ – это обозначения восстановленных форм коферментов.
НАДН, Н+ и ФАДН2 переносят водород
от субстратов в ДЦ (для выработки АТФ),
а НАДФН, Н+ переносит водород от метаболитов ПФП не в ДЦ,
а в реакции,
катализируемые редуктазами и гидроксилазами.
Дегидрогеназы катализируют реакции
процессов окислительного катаболизма.
См. п.32, 45, 65.
2. О К С И Д А З Ы
катализируют дегидрирование,
при котором водород, отщепленный от субстрата, присоединяется к кислороду (О2).
Формулируя короче – дегидрогеназы переносят 2 атома водорода
от субстрата на кислород.
Схема реакции, которая катализируется оксидазами,
может быть представлена в таком виде:
RH2 + О2 ; R + Н2О2.
Где RH2 – это восстановленный субстрат,
R – окисленный субстрат
(органический субстрат после отщепления от него водорода).
Кислород в результате этой реакции восстанавливается.
Для работы оксидоредуктаз нужен кофермент ФАД
и витамин В2 в составе ФАД.
Основные примеры оксидаз –
это ксантин/оксидаза (КсО) в п.71
и моноамин/оксидаза (МАО) в п.105.
КсО участвует в катаболизме пуринов
(аденина и гуанина,
но субстраты КсО – гипоксантин и ксантин;
под действием КсО гипоксантин превращается в ксантин,
а ксантин – в мочевую кислоту).
МАО участвует в окислении аминов (адреналина, например).
Ингибиторы КсО применяются для снижения выработки уратов (см. гипер/урикемии),
а ингибиторы МАО применяются в качестве антидепрессантов.
Оксидазы участвуют в реакциях свободного окисления – п.26.
Сходство и отличия дегидрогеназ и оксидаз:
сходство в том, что катализируют отщепление водорода (дегидрирование),
отличия в том, что
дегидрогеназы переносят отщеплённый от субстратов водород на коферменты,
а оксидазы – на кислород (окси).
катализируют включение в молекулу органического субстрата
атомов кислорода, источником которых является О2.
Атомы кислорода включаются
между атомом водорода органического субстрата
и атомом углерода субстрата,
поэтому молекула органического субстрата
до включения в нее атомов кислорода оксигеназами обозначается так – RН,
а после включения атомов кислорода –
либо R-О-О-Н (если включены оба атома О2),
либо R-О-Н (если включен один атом О2).
3.1). Оксигеназы, которые включают в молекулу субстрата
оба атома кислорода,
называются ДИоксигеназами;
схему реакции можно записать так:
Продукт реакции (R-О-О-Н)
называется органической перекисью.
RООН – более окисленное вещество, чем RН,
то есть окисляется органический субстрат,
а восстанавливается кислород.
3.2). Оксигеназы, которые включают в молекулу органического субстрата
только один атом кислорода,
называются МОНОоксигеназами или гидроксилазами.
Второй атом кислорода молекулы кислорода
соединяется с двумя атомами водорода, образуя молекулу воды;
источником атомов водорода в этом случае является кофермент –
либо НАДФН, либо аскорбат.
Схему реакции можно записать так:
RH + О2 + КоФН2 ; R-О-Н + КоФ + Н2О.
RН – это субстрат, в который должен включиться атом кислорода,
R-О-Н – это субстрат со включенным в него атомом кислорода,
О2 – это источник атомов кислорода,
КоФН2 – это источник атомов водорода.
Субстрат RН – более восстановленный по сравнению с RОН.
В реакции окисляются RН и КоФН2,
а восстанавливается кислород.
-ОН – это спиртовая (гидроксильная) группа,
а RОН – это спирт.
Из-за того, что при действии монооксигеназ
образуется гидроксильная группа,
у них есть синоним – гидроксилазы. (Не путать с гидролазами.)
Нужно уметь написать реакции,
которые катализируют фенилаланин/гидроксилаза
и тирозин/гидроксилаза (п.105 и 68).
И знать значение этих реакций.
Оксигеназы (как и оксигеназы),
участвуют в процессах свободного окисления.
Участвуют в метаболизме ксенобиотиков,
в обмене многих гормонов,
в образовании коллагена.
катализируют присоединение водорода
к органическому субстрату,
при этом источником атомов водорода является НАДФН.
Другой вариант определения –
редуктазы катализируют перенос водорода
от кофермента на органический субстрат.
Действие редуктаз противоположно действию дегидрогеназ.
При получении водорода субстрат восстанавливается,
поэтому редуктазы можно считать восстановителями субстратов.
Схема реакций, которые катализируются редуктазами:
Здесь R – органический субстрат до присоединения водорода,
RН2 – органический субстрат после присоединения к нему атомов водорода,
КоФ2 – восстановленная форма кофермента (источник водорода),
КоФ – окисленная форма кофермента.
В этой реакции органический субстрат восстанавливается (приобретает водород),
а кофермент окисляется (теряет водород).
Редуктазы – основные ферменты восстановительных синтезов –
например, синтеза жирных кислот,
синтеза холестерина (ГМГ-КоА/редуктаза),
синтеза дезокси/рибонуклеотидов (рибонуклеотид/редуктаза).
А глутатион/редуктаза относится к антиокислительным ферментам – п.27.
5. Ц И Т О Х Р О М Ы
участвуют в реакциях изменения валентности металлов –
например, в присоединении электрона к иону железа Fe3+.
В результате ион железа Fe3+превращается в ион железа Fe2+
(восстановление иона железа).
Схема реакции: Fe3+ + е ; Fe2+.
Почему (3+) превращается в (2+) при присоединении электрона – потому что у электрона отрицательный заряд.
Получается (3+) + (1-) = (2+).)
В каких процессах встречаются цитохромы –
цитохромы катализируют ряд реакций дыхательной цепи – п.22;
нужно также помнить цитохром Р 450 – п.118.
6. А Н Т И О К И С Л И Т Е Л Ь Н Ы Е Ф Е Р М Е Н Т Ы .
См. п.27.
Это ферменты, которые участвуют в разрушении активных форм кислорода
и восстановлении окисленных ими веществ клетки
(органических перекисей).
Относятся к антиокислительной системе организма,
к которой также относятся низкомолекулярные антиоксиданты
(витамины А, Е, С и другие).
Благодаря этой системе организм дольше сохраняет молодость
и дольше не появляются такие болезни, как атеросклероз, катаракта и т.д..
Подробнее об антиокислительных ферментах сказано в ответе на вопрос № 27.
Примеры антиокислительных ферментов –
супероксид/дисмутаза,
глутатион/пероксидаза, глутатион/трансфераза,
глутатион/редуктаза, каталаза.
Реакции, катализируемые оксидоредуктазами,
можно разделить на группы –
к одной группе относятся оксидоредуктазы,
которые катализируют восстановление органических субстратов
(редуктазы = восстановители),
а к другой – оксидоредуктазы, которые катализируют
окисление органических субстратов (все, кроме редуктаз).
Оксидоредуктазы, которые катализируют реакции окисления органических субстратов,
можно разделить на три группы:
1) катализирующие отщепление водорода
(дегидрирование) дегидрогеназы и оксидазы,
2) катализирующие присоединение кислорода
(оксигенацию) оксигеназы,
3) катализирующие изменение валентности металлов цитохромы.
Как определить, какая форма субстрата более восстановленная,
а какая – более окисленная:
чем больше водорода в веществе,
тем более восстановлено вещество;
чем больше кислорода в веществе,
тем более окисленное вещество.
источник
| Структурная формула, рациональное название и буквенное обозначение | Перенос | Тип |
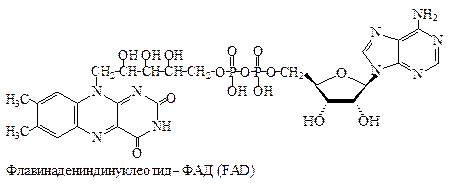 | 2ē и 2Н + | П |
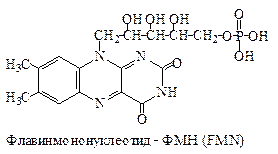 | 2ē и 2Н + | П |
ФМНи ФАД ковалентно связаны с ферментами. Активной группой обоих коферментов является флавин (изоаллоксазин), имеющий сопряженную систему из трех колец, которая может при восстановлении принимать два электрона и два протона.
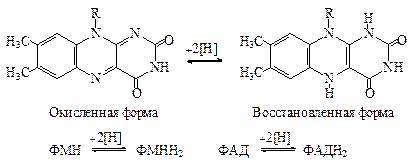
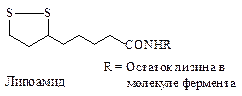 | 2ē и 2Н + | П |
Влипоамиде функцию окислительно-восстановительного центра выполняет внутримолекулярный дисульфидный мостик. Липоевая кислота ковалентно связана с остатком лизина молекулы фермента.
Остаток липоевой кислоты прежде всего участвует в окислительном декарбоксилировании 2-кетокислот.
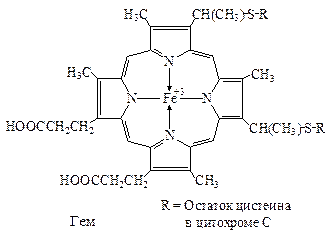 | 1ē | П |
Группагемаявляется окислительно-восстановительным коферментом в дыхательной цепи, фотосинтезе, а также в монооксигеназах и пероксидазах.
В отличие от гемоглобина в этих случаях ион железа меняет валентность.
Гем в цитохроме С, ковалентно связан с двумя остатками цистеина молекулы фермента.
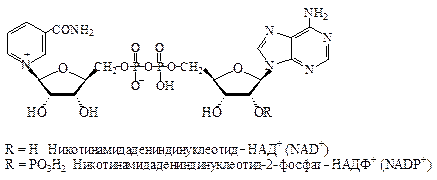 | 2ē и 1Н + | P |
Коферменты НАД + иНАДФ + широко распространены как коферменты дегидрогеназ. Они переносят гидрид-ион(Н ‾ ) и действуют всегдав растворимой форме.
НАД + передает восстановительный эквивалент из катаболического пути в дыхательную цепь и тем самым участвует в энергетическом обмене. НАДФ + , напротив, является самым важным восстановителемпри биосинтезе.
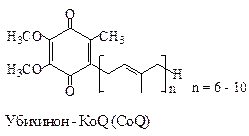 | 2ē и 2Н + | Р |
Убихинонявляется переносчиком восстановительных эквивалентовв дыхательной цепи. При восстановлении хинон превращается в ароматический гидрохинон(убихинол).
Аналогичные системы хинон/гидрохинон принимают участие в реакциях фотосинтеза. К этому классу окислительно-восстановительных систем принадлежат также витамины Е и К.
Из сопоставления таблиц 1 и 2, видно, что такие витамины как рибофлавин, липоевая кислота, липоамид, никотиновая кислота и никотинамид являются предшественниками коферментов оксидоредуктаз.
Гем в чистом виде не применяется в медицинской практике из-за сложности его выделения и синтеза. В качестве препарата, содержащего гем, в медицине применяется препарат крови — «гематоген».
Хотя методы синтеза убихинонов разработаны, до настоящего времени окончательно не установлены пути их биосинтеза. Коферменты Q6–Q9 обнаружены в различных микроорганизмах, а кофермент Q10 в человеческом организме. Интересно отметить, что кофермент Q10 в последнее время нашел применение в косметологии.
Аскорбиновую кислоту также целесообразно отнести к растворимому коферменту, поскольку она принимает участие в реакциях окисления некоторых субстратов кислородом, главным образом в реакциях гидроксилирования. Из биохимических процессов с участием аскорбиновой кислоты следует отметить окисление тирозина, синтезы катехоламинов и желчных кислот. Она является коферментом фермента проколлагенпролин-4-диоксигеназы, катализирующего окисление остатков пролина, входящих в структуру проколлагена, до 4-гидроксипролина в процессе созревания коллагена (Аминокислоты и полипептиды: учеб. пособ. Ч. I./ В.А. Смирнов, Ю.Н. Климочкин. – Самара. Самар. гос. техн. ун-т., 2007, стр.10).
В таблице 3 приведены структурные формулы, названия и буквенные обозначения коферментов, участвующих в реакциях переноса функциональных групп, а также соответствующие ферменты и переносимые ими группы.
Последнее изменение этой страницы: 2017-01-24; Нарушение авторского права страницы
источник
КЛАССИФИКАЦИЯ И НОМЕНКЛАТУРА ФЕРМЕНТОВ
Современная классификация ферментов разработана Международным биохимическим союзом (1961г.). В ее основу положен тип катализируемой реакции и механизм. Все ферменты делят на шесть классов: I. Оксидоредуктазы. II. Трансферазы. III. Гидролазы. IV. Лиазы. V. Изомеразы. VI. Лигазы.
Каждый фермент имеет кодовый номер по классификации ферментов: первая цифра характеризует класс реакции, вторая − подкласс, третья − подподкласс, четвертая цифра указывает порядковый номер фермента в его подподклассе. Название фермента состоит из двух частей: в первой части − название субстрата (или субстратов), во второй − тип катализируемой реакции.
Оксидоредуктазы катализируют окислительно-восстановительные реакции и подразделяются на 5 основных подклассов:
Оксидазы. Катализируют удаление водорода из субстрата, используя при этом в качестве акцептора водорода только кислород. Оксидазы содержат медь, продуктом реакции является вода (исключение составляют реакции, катализируемые уриказой и моноаминоксидазой, в результате которых образуется Н2О2).
Общая схема процесса следующая:
В качестве субстратов оксидаз могут выступать фенолы, полифенолы, амины. Примерами ферментов класса оксидаз являются фенолаза, цитохром-оксидаза, моноаминоксидаза, уриказа.
Фенолаза (катехолоксидаза, тирозиназа) − медьсодержащий фермент с широкой специфичностью. Он катализирует превращение монофенола
(в присутствии о-дифенола) в орто-хинон. Медь содержится также в уриказе, катализирующей окисление мочевой кислоты в аллантоин, и в моноаминоксидазе, окисляющей адреналин и тирамин в митохондриях.
Цитохромоксидаза − гемопротеин, который служит конечным компонентом дыхательной цепи и осуществляет перенос электронов на конечный акцептор − кислород. Данный фермент ингибируется оксидом углерода (II), цианидами и сероводородом. Фермент содержит две молекулы гема, в каждой из которых атом железа может переходить из состояния Fe 2+ в состояние Fe 3+ и обратно в ходе окисления и восстановления, а также два атома Сu, каждый из которых взаимодействует с одним из гемов.
Аэробные дегидрогеназы. Катализируют удаление водорода из суб-страта, используя в качестве акцептора водорода не только кислород, но и искусственные акцепторы (например, метиленовый синий). Эти дегидрогеназы относятся к флавопротеинам.
В результате реакции образуется пероксид водорода, а не вода:
В качестве кофермента дегидрогеназы содержат ФАД (флавинаденин-динуклеотид) или ФМН (флавинмононуклеотид). Многие флавопротеиновые ферменты содержат несколько ионов металлов.
К ферментам группы аэробных дегидрогеназ относятся: дегидрогеназа L-аминокислот (оксидаза L-аминокислот), катализирующая окислительное дезаминирование природных L-аминокислот, и ксантиндегидрогеназа (ксантиноксидаза), катализирующая окисление ксантина в мочевую кислоту. Молибденсодержащий фермент ксантиноксидаза играет важную роль в катаболизме пуриновых оснований.
Анаэробные дегидрогеназы. Катализируют удаление водорода из субстрата, но не способны использовать кислород в качестве акцептора.
Общая схема процесса следующая:
Анаэробные дегидрогеназы подразделяются в зависимости от природы кофермента на несколько групп.
НАД + -зависимые (пиридинзависимые, первичные) дегидрогеназы, содержащие в качестве кофермента НАД + или НАДФ + . В общем случае НАД + -зависимые дегидрогеназы катализируют окислительно-восстановительные реакции специфических (например, гликолиза) и общих путей катаболизма (например, цикла Кребса, дыхательной цепи).
Общая схема процесса следующая:
Примером НАД + -зависимых дегидрогеназ могут служить лактатдегидрогеназа, алкогольдегидрогеназа, глутаматдегидрогеназа и др. Например, 1.1.1.27 L-лактат: НАД + -оксидоредуктаза (лактатдегидрогеназа) катализирует взаимопревращение лактата и пирувата:
ФАД- и ФМН- зависимые анаэробные дегидрогеназы (флавин-зависимые дегидрогеназы). Первичные флавинзависимые дегидрогеназы переносят восстановительные эквиваленты от субстрата непосредственно на дыхательную цепь. К ним относятся, например, 1.3.99.1 сукцинатдегидрогеназа (СДГ), ацил-КоА-дегидрогеназа и митохондриальная глицерол-3-фосфат-дегидрогеназа:
Вторичная ФМН-зависимая НАДН-дегидрогеназа − компонент дыхательной цепи, переносящий электроны от НАДН к более электроположительным компонентам:
Еще одна функция флавинзависимых дегидрогеназ − катализируемое дигидролипоилдегидрогеназой дегидрирование восстановленного липоата
(промежуточного продукта при окислительном декарбоксилировании пирувата и a-кетоглутарата). При этом вследствие низкого значения окислительно-восстановительного потенциала системы липоата переносчиком водорода от восстановленного липоата к НАД + является флавопротеин (ФАД).
Цитохромы за исключением цитохромоксидазы классифицируются как анаэробные дегидрогеназы. В дыхательной цепи они служат переносчиками электронов от флавопротеинов к цитохромоксидазе. Цитохромы являются гемопротеинами, у которых атом железа переходит из состояния Fe 2+ в Fe 3+ и обратно в процессе окисления и восстановления. Помимо дыхательной цепи цитохромы имеются в эндоплазматическом ретикулуме (цитохромы Р-450 и b-5).
Гидропероксидазы. К их числу относятся ферменты пероксидаза и каталаза.
Пероксидаза − фермент, катализирующий окисление пероксидом водорода различных органических соединений − фенолов, аминов, аскорбиновой кислоты, цитохрома С. Пероксидаза обнаружена в растениях, молоке, лейкоцитах, тромбоцитах, а также в тканях, в которых происходит метаболизм эйкозаноидов. Фермент содержит протогем, который в отличие от гемовых групп большинства гемопротеинов слабо связан с апоферментом.
Реакция, катализируемая пероксидазой, имеет сложный характер; суммарная реакция выглядит следующим образом:
В эритроцитах глутатионпероксидаза, содержащая в качестве простетической группы селен, катализирует разложение Н2О2 и гидропероксидов липидов восстановленным глутатионом и, таким образом, защищает липиды мембран и гемоглобин от окисления пероксидами.
Каталаза − это гемопротеин, содержащий 4 гемовые группы. Наряду с пероксидазной активностью каталаза способна использовать одну молекулу Н2О2 в качестве донора электронов, а другую − в качестве акцептора электронов. В организме каталаза в основном разлагает пероксид водорода, образующийся при действии аэробных дегидрогеназ:
Каталаза содержится в крови, костном мозге, мембранах слизистых оболочек, почках и печени.
Во многих тканях, включая и печень, обнаружены микротельца − пероксисомы, которые богаты аэробными дегидрогеназами и каталазой. Биологически выгодно группировать в одном месте как ферменты, приводящие к образованию Н2О2, так и ферменты, разлагающие это соединение.
К ферментам, катализирующим образование Н2О2, кроме пероксисомных ферментов, относятся также митохондриальные и микросомные системы транспорта электронов.
Ферменты этой группы катализируют включение кисло-рода в молекулу субстрата, которое происходит в две стадии:
1) кислород связывается с активным центром фермента;
2) происходит реакция, в результате которой, связанный кислород восстанавливается или переносится на субстрат.
Оксигеназы не относятся к ферментам, которые катализируют реакции, снабжающие клетку энергией; они участвуют в синтезе и деградации многих типов метаболитов, токсинов и ксенобиотиков. Оксигеназы подразделяются на 2 подгруппы.
Монооксигеназы (гидроксилазы). Эти ферменты катализируют включение в субстрат только одного из атомов молекулы кислорода. Другой атом кислорода восстанавливается до воды; для чего необходим дополнительный донор электронов (косубстрат):
Природа косубстрата может быть различной. Многие оксигеназы используют НАДФН2. В этом случае суммарное уравнение реакции можно записать как
К подобным системам относятся микросомные цитохром-Р-450-содержащие монооксигеназные системы, участвующие в метаболизме многих лекарственных веществ путем их гидроксилирования. Они находятся в микросомах печени вместе с цитохромом Р-450 и цитохромом b-5. Восстановителями этих цитохромов являются НАДН и НАДФН. Цитохромы окисляются субстратами в результате серии ферментативных реакций, составляющих так называемый гидроксилазный цикл:
Лек — лекарственное вещество
К лекарственным веществам, метаболизм которых идет при участии рассматриваемых систем, относятся, например, морфин и бензпирен. Многие лекарственные вещества (например, фенобарбитал) способны индуцировать синтез микросомных ферментов и цитохрома Р-450. Цитохром Р-450 является одновременно гемо- и флавопротеином, причем флавиновые нуклеотиды выступают в качестве второго донора электронов. Цитохром Р-450 в печени осуществляет гидроксилирование липофильных соединений, образующихся в качестве побочных продуктов или попадающих в организм извне (такие вещества объединяют под общим названием «ксенобиотики»). Введение в их молекулы гидроксильных групп повышает гидрофильность этих веществ, понижает токсичность и облегчает их вывод из организма.
Другой пример подобных систем − митохондриальные цитохром-Р-450-содержащие монооксигеназные системы. Они находятся в коре надпочечников, семенниках, яичниках, плаценте, почках и участвуют в биосинтезе стероидных гормонов из холестерина, катализируют гидроксилирование гидроксихолекальциферола, что приводит к образованию активной формы витамина D3 (1,25-дигидроксихолекальциферола). В коре надпочечников содержание митохондриального цитохрома Р-450 в 6 раз выше, чем содержание цитохромов в дыхательной цепи.
Диоксигеназы (истинные оксигеназы). Эти ферменты катализируют включение в молекулу субстрата обоих атомов молекулы кислорода:
Примером служат железосодержащие ферменты 1.13.11.5 гомогентизатдиоксигеназа и 1.13.11.6 3-гидроксиантранилатдиоксигеназа, а также некоторые гемсодержащие ферменты, в частности триптофандиоксигеназа (триптофанпирролаза).
Не нашли то, что искали? Воспользуйтесь поиском:
источник
Классификация ферментов.
Микросомальная система гидроксилирования
(сокращенная форма методического пособия — ЭНЗИМОЛОГИЯ)
для студентов 2-го курса лечебного, педиатрического и стоматологического факультетов.
Классификация ферментов
В зависимости от типа катализируемой реакции выделяют 6 классов ферментов.
Рабочее название фермента строится так: название субстрата + подкласс фермента.
| Класс | Тип катализируемой реакции |
| Оксидоредуктазы | Окислительно-восстановительные реакции. |
| Трансферазы | Перенос отдельных групп атомов от донорной молекулы к акцепторной молекуле. |
| Гидролазы | Гидролитическое (с участием воды) расщепление связей. |
| Лиазы | Расщепление связей способом, отличным от гидролиза или окисления. |
| Изомеразы | Взаимопревращение различных изомеров. |
| Лигазы (синтетазы) | Образование связей в реакции конденсации двух различных соединений (используется энергия АТР). |
класс – оксидоредуктазы
— катализируют окислительно-восстановительные реакции.
а) Дегидрогеназы отщепляют водород от молекулы субстрата.
Дегидрогеназы разделяют на пиридиновые и флавиновые.
Пиридиновые дегидрогеназы, в качестве кофермента содержат НАД + (NAD + ) или НАДФ + (NADP + ). НАД – никотинамид аденин динуклеотид.
Пример: реакция окисления этилового спирта:
Пример: реакция окисления соли яблочной кислоты (малата):
Рабочее название дегидрогеназ строится так: название субстрата (восстановленная форма) + дегидрогеназа.
Флавиновые дегидрогеназы в качестве простетической группы содержат ФАД.
Пример: реакция окисления соли янтарной кислоты (сукцината):
Дегидрогеназы бывают аэробные и анаэробные. Аэробные дегидрогеназы отдают атомы водорода кислороду с образованием перекиси водорода:
Пиридиновые дегидрогеназы, как правило, анаэробные, а флавиновые бывают и аэробные и анаэробные. Дегидрогеназы бывают первичные и вторичные . Первичные окисляют небелковый субстрат. Вторичные – белковый. Обычно они окисляют другую дегидрогеназу. Реакция выглядит так: НАДНН + +ФАД→ФАДН2+НАД +
б) Цитохромы — это гемсодержащие ферменты, они переносят электроны. Цитохромы участвуют в тканевом дыхании и микросомальном окислении. Они бывают аэробные и анаэробные. В качестве аэробных цитохромов можно привести пример цитохрома Р450 микросомальной системы гидроксилирования.
Пример: реакция окисления дофамина до норадреналина
Пример: :реакция окисления фенилаланина до тирозина
г) Пероксидазы расщепляют перекиси. В качестве примера можно привести:
Эти ферменты защищают наш организм от токсичных форм кислорода.
Класс – трансферазы
-переносят группы с одного субстрата на другой или обмен группами между субстратами. В зависимости от того, какие группы переносят трансферазы их разделяют на подклассы:
В качестве примера приведем:
Аминатрансферазу : обмен амино- группы на кето- группу (реакция трансаминирования)
Фосфотрансфераза (киназа). Фосфатная группа переносится с АТФ на субстрат.
Класс – гидролазы
— катализируют реакции гидролиза (распада веществ под действием воды). В зависимости от вида связи гидролазы подразделяются на подклассы.
а) эстеразы –гидролиз сложноэфирных связей
б) фосфоэстеразы – гидролиз фосфоэфирных связей
в) пептидазы – гидролиз пептидных связей.
г) гликозидазы –гидролиз гликозидных связей между молекулами углеводов.
В качестве примера приведем ацетилхолинэстеразу .
Класс –лиазы
— катализируют реакции распада веществ без участия воды). В зависимости от вида связи гидролазы подразделяются на подклассы.
Класс – изомеразы
— катализируют реакции изомеризации.
изомераза глюкоза-6- фосфат
Класс – синтетазы
— катализируют реакции синтеза веществ с затратой АТФ.
Синтетаза щавелевоуксусной кислоты
Название синтетаз строится так: Синтезируемое соединение +синтетаза.
источник
Более двух десятилетий назад, Doll и Peto (The causes of cancer: quantitative estimates of avoidable risks of cancer in the United States today) показали, что 35% всех случаев смерти от рака в Соединенных Штатах и Европе может быть предотвращено с помощью изменений в диете, это на 5% больше, чем для табака и на 25% больше, чем для инфекций.
Это говорит о том, что питание, являющееся неотъемлемой частью нашей жизни, важно не только для нашей фигуры, здоровья сердечно-сосудистой системы и интеллектуального долголетия, но и для защиты от онкологической патологии.
Остановимся подробнее на отдельных составляющих нашего привычного рациона, для этого заглянем в настольную книгу современного онколога Devita, Hellman, and Rosenberg’s cancer: principles & practice of oncology.
Наиболее важное влияние диеты на риск развития рака опосредовано массой тела. Избыточный вес, ожирение и пассивный образ жизни являются основными факторами риска развития рака.
В большом исследовании Американского онкологического общества, тучные люди имели значительно более высокую смертность от всех видов рака и, в частности, от колоректального рака, рака молочной железы в постменопаузе, рака тела матки, рака шейки матки, рака поджелудочной железы и рака желчного пузыря, чем у их сверстников с нормальной массой тела.
Ожирение и, в частности, окружность талии являются предикторами заболеваемости раком толстой кишки у женщин и мужчин. Увеличение веса на 10 кг или более связано со значительным увеличением в постменопаузе заболеваемости рака молочной железы среди женщин, которые никогда не использовали заместительную гормональную терапию, в то время как потеря веса после менопаузы существенно уменьшает риск рак молочной железы. Избыточный вес тесно связан с эндогенным уровнем эстрогена, который, вероятно, способствует избыточному росту эндометрия и риску рака молочной железы в постменопаузе.
Причины возникновения других видов рака менее ясна, но избыточный вес тела также связан с более высоким уровнем циркулирующего инсулина, инсулиноподобного фактора роста (IGF) -1, и С-пептида (маркер секреции инсулина), низким уровнем связывания белков с половыми гормонами и IGF-1, а также с более высокими уровнями различных воспалительных факторов, все из которых могут гипотетические быть связаны с риском развития различных видов рака.
Международным агентством по изучению рака алкоголь классифицируется как канцероген. Потребление алкоголя увеличивает риск многочисленных видов рака, в том числе печени, пищевода, глотки, полости рта, гортани, молочной железы и колоректального рака в зависимости от дозы.Фактические данные доказывают, что чрезмерное потребление алкоголя увеличивает риск первичного рака печени, возможно, через цирроз и алкогольный гепатит.
Механизмы могут включать в себя прямое повреждение клеток в верхних отделах желудочно-кишечного тракта; модуляцию метилирования ДНК, который влияет на восприимчивость ДНК к мутациям; и увеличению количества ацетальдегида, основного метаболита спирта, который усиливает пролиферацию эпителиальных клеток, образуют агенты, повреждающие ДНК, и является признанным канцерогеном.
Связь между потреблением алкоголя и раком молочной железы примечательна тем, что небольшой, но значительный риск был обнаружен даже при потреблении одного напитка в день. Механизмы могут включать в себя взаимодействие с фолиевой кислотой, увеличение уровня эндогенных эстрогенов, и повышение концентрации ацетальдегида.
Интерес к пищевому жиру в качестве причины раки начался в первой половине 20-го века, когда исследования “Танненбаум” показали, что диета с высоким содержанием жира может способствовать росту опухоли у животных. Особенно сильные корреляции были замечены с риском развития рака молочной железы, толстой кишки, простаты и эндометрия, которые являются наиболее важными видами рака не по причине курения в развитых странах.
Эти корреляции были характерны для животного жира (особенно для красного мяса), но не для растительного жира.
Фрукты и овощи гипотетически должны вносить существенный вклад в профилактику рака, потому что они богаты веществами, обладающими потенциально противораковыми свойствами. Фрукты и овощи содержат антиоксиданты и минералы и являются хорошими источниками клетчатки, калия,каротиноидов, витамина С, фолиевой кислоты и других витаминов.
Несмотря на то, что фрукты и овощи составляют менее 5% от общего калоража в большинстве стран по всему миру, концентрация микроэлементов в этих продуктах больше, чем в большинстве других.
Связь между потреблением фруктов и овощей и заболеваемостью раком толстой или прямой кишки рассматривалась по крайней мере в шести крупных исследованиях. В некоторых из этих проспективных исследований наблюдалась обратная зависимость для отдельных продуктов или подгруппы фруктов или овощей.
Результаты крупнейшего исследования среди медсестер “Health Study”и среди медицинских работников “Follow-Up Study” не показывают никакой важной связи между потреблением фруктов и овощей и уменьшением количества случаев рака толстой или прямой кишки во время 1,743,645 наблюдений. В этих двух больших популяциях диета постоянна анализировалась в течение периода наблюдения с помощью подробного анкетирования участников об их каждодневном рационе.
Аналогичным образом, в проспективном исследовании “Pooling Project”, включающем 14 исследований, 756217 участников и 5838 случаев рака толстой кишки, никакой связи с общим риском развития рака толстой кишки не было найдено.
Анализ исследований Health Study и Follow-Up Study, включающих более 9000 случаев заболевания раком, не выявил существенной пользы потребления фруктов и овощей для общей заболеваемости раком. Несмотря на то, что обильное потребление овощей и фруктов не может снизить риск развития опухолей, тем не менее есть существенная польза для защиты организма от сердечно-сосудистых заболеваний.
Под термином “пищевые волокна” с 1976 года понимается “совокупность всех полисахаридов растений и лигнин, которые устойчивы к гидролизу пищеварительными ферментами человека”. Волокна, как растворимые, так и нерастворимые, ферментируются просветными бактериями толстой кишки.
Среди всех свойств волокон, важным для профилактики рака являются их эффект «набухания», что сокращает время прохождения химуса по ободочной кишке и позволяет связывать потенциально канцерогенные химические вещества. Волокна могут также помогать просветным бактериям в производстве жирных кислот с короткой цепью, которые могут непосредственно обладать антиканцерогенными свойствами.
Некоторые исследователи считают, что пищевые волокна могут снизить риск развития рака молочной железы за счет снижения кишечной абсорбции эстрогенов и прохождения их через билиарную систему.
Регулярное потребление молока связано с незначительным снижением риска развития колоректального рака, что было показано в крупном мета-анализе когортных исследований, возможно из-за содержания в нём кальция. По результатам нескольких рандомизированных исследований, добавление кальция в рацион снижает риск развития колоректального рака и аденом.
С другой стороны, в нескольких исследованиях высокое потребление кальция или молочных продуктов было ассоциировано с повышенным риском рака простаты, в частности, со смертельным исходом рака простаты. Употребление трех или более порций молочных продуктов продуктов в день было связано с раком эндометрия у женщин в постменопаузе, не использующих гормональную терапию.
Высокое потребление лактозы из молочных продуктов также было связано с умеренно высоким риском развития рака яичников.
В 1980 году Гарленд выдвинул гипотезу, что солнечный свет и витамин D может снизить риск развития рака толстой кишки. С тех пор, существенное количество исследований было проведено по поводу обратной связи между циркулирующим 25-гидроксивитамином D(25 [OH] D) и риском колоректального рака. Было показано, что уровень витамина D может, в частности влиять на прогноз колоректального рака; смертность от колоректального рака составила на 72% ниже среди лиц с концентрацией 25 (OH) D 80 нмоль / л или выше.
Высокая плазменная концентрация витамина D связаны с уменьшением риска развития некоторых других видов рака, включая рак молочной железы, простаты, особенно со смертельным исходом, и яичника.
Вышеизложенные факты доказывают, что в мире онкологии вопрос о рациональном и профилактическом питании остаётся открытым. Однако, на основании уже имеющихся данных мы можем сформулировать некоторые рекомендации, сформулированные Американским Обществом против рака:
- Не пренебрегайте регулярными физическими нагрузками. Физическая активность является основным способом контроля веса, а это, как мы уже выяснили, снижает риск развития некоторых видов рака, особенно рака толстой кишки.
- Избегайте избыточного веса. Положительный энергетический баланс приводит к избыточному отложению жира в организме, что является одним из наиболее важных факторов риска развития рака.
- Ограничьте потребление алкоголя. Это способствует уменьшению риска развития многих видов рака, а также уменьшает смертность (в том числе и онкологических больных) от несчастных случаев.
- Потребляйте много фруктов и овощей. Частое потребление фруктов и овощей во взрослой жизни, вероятно, не играет существенной роли в заболеваемости раком, но уменьшает риск развития сердечно-сосудистых заболеваний.
- Потребляйте цельное зерно и избегайте рафинированных углеводов и сахаров. Регулярное потребление цельного зерна вместо продуктов из рафинированной муки и низкое потребление рафинированного сахара снижает риск развития сердечно-сосудистых заболеваний и диабета.
- Замените красное мясо рыбой, орехами и бобовыми, ограничьте потребление молочных продуктов. Потребление красного мяса увеличивает риск развития колоректального рака, диабета и ишемической болезни сердца, и должно быть в значительной степени снижено. Частое потребление молочных продуктов может увеличить риск развития рака простаты. Рыба, орехи и бобовые являются отличными источниками моно- и полиненасыщенных жиров и растительных белков и может способствовать снижению темпов развития сердечно-сосудистых заболеваний и диабета.
- Рассмотрите вопрос о потреблении добавок с витамином D. Значительная часть населения, особенно тех, кто живет в более высоких широтах, испытывают дефицит витамина D. Большинство взрослых людей могут извлечь пользу от принятия 1000 МЕ витамина D3 в день в течение месяца при низкой интенсивности солнечного света. Витамин D будет, как минимум, снижать частоту переломов костей, и, вероятно, частоту рака ободочной и прямой кишки.
Подробнее с этими и многими другими рекомендациями можно ознакомиться в оригинальной статье American Cancer Society Guidelines on nutrition and physical activity for cancer prevention: reducing the risk of cancer with healthy food choices and physical activity.
1) Devita, Hellman, and Rosenberg’s cancer : principles & practice of oncology / editors, Vincent T. DeVita, Jr.,Theodore S. Lawrence, Steven A. Rosenberg ; with 404 contributing authors.—10th edition.
2) Doll R, Peto R. The causes of cancer: quantitative estimates of avoidable risks of cancer in the United States today. J Natl Cancer Inst 1981
3) Kushi LH, Doyle C, McCullough M, et al. American Cancer Society Guidelines on nutrition and physical activity for cancer prevention: reducing the risk of cancer with healthy food choices and physical activity. CA Cancer J Clin 2012.
источник
Оксидоредуктазы катализируют окислительно-восстановительные реакции.
При этом происходит перенос атомов водорода или но отдельности протонов и электронов. Схематично действие оксидоредуктаз можно описать уравнением:
Если S, — это нс кислород, то процесс анаэробный, а ферменты называют дегидрогеназами, если S, — кислород, то процесс аэробный, а ферменты в зависимости от условий называют оксидазами или оксигеназами.
Оксидоредуктазы — многочисленный класс ферментов. Их насчитывают более 500. Они являются двухкомпонентными. При такой большой численности оксидоредуктаз набор их кофсрментов довольно ограничен, а субстратная специфичность обусловлена строением белковой части фермента.
Международные названия строятся по принципу:
Наиболее распространены никотинамидные (пиридинзависимые) ко- ферменты. Такое название они получили благодаря амиду никотиновой кислоты (никотинамиду, он же витамин В5), в структуру которого входит гетероцикл пиридин. В составе кофермента есть также азотистое основание аденин и остатки рибозы, соединенные дифосфатной группировкой. Весь кофермент представляет собой объединение двух нуклеотидов. Поэтому полное название кофермента — никотинамидадеииндинуклеотид (НАД) или пикотинамидадениндинуклеотидфосфат (НАДФ).
Разница в строении обусловливает разную локализацию ферментов, содержащих НАД и НАДФ, и взаимодействие с различными субстратами.
Рис. 6.17. Строение коферментов:
В катализируемой реакции проявляет активность непосредственно амид никотиновой кислоты (рис. 6.18).
Рис. 6.18. Работа активного центра НАД и НАДФ
Более половины известных в настоящее время оксидоредуктаз содержат НАД или НАДФ в качестве кофермента.
Флавинзависимые оксидоредуктазы или флавопротеины. Их кофермен- тами являются флавинмононуклеотид (ФМН) (рис. 6.19) или флавинаде- ниндинуклеотид (ФАД) (рис. 6.20).
Активным центром этих коферментов является флавиновый комплекс, который получил свое название за желтый цвет (от греч. flavus — желтый). Как очевидно из рис. 6.21, флавиновые коферменты обратимо переносят атомы Н.
Большинство флавопротеипов — вторичные дегидрогеназы, по некоторые флавопротеины, особенно с ФАД в качестве кофермента, могут пепо-
Рис. 6.19. Структура ФМН
Рис. 6.20. Структура ФАД
Рис. 6.21. Работа активного центра ФАД и ФМН
средственно снимать атомы водорода с субстрата, т.е. являются первичными дегидрогеназами.
Коферментами оксидоредуктаз являются хиноны. В животных организмах — это убихинон (рис. 6.22), а в растительных — пластохинон. Другое их название — кофермент Q. В боковой ветви кофермента Q находятся повторяющиеся 6—10 раз остатки изопрена. Отсюда еще одно название — Ql0. Именно длинная боковая ветвь придает высокую гидрофобность этому ко- ферменту, благодаря чему он легко встраивается в липидный слой мембран.
Рис. 6.22. Участие KoQ. в окислительно-восстановительной реакции
Некоторые оксидоредуктазы в качестве простетической группы содержат липоевую кислоту, которая получила название за липофильные свойства — способность растворяться в органических соединениях и нерастворимость в воде, благодаря чему может легко проникать через различные биомембраны.
Роль липоевой кислоты важна в превращении ПВК в ацетил-КоА (см. рис. 6.13), т.е. в утилизации углеводов. Также липоевая кислота обладает выраженными антиоксидантными свойствами как в жирорастворимых, так и в водорастворимых средах, прерывая свободнорадикальные процессы.
Активную роль при этом играют тиольные (сульфгидрильпые) SH-rpyn- пы (рис. 6.23), поэтому липоевую кислоту относят также к группе тиоль- ных коферментов. Благодаря макроэргической связи, образуемой между атомом S и субстратом, липоевая кислота осуществляет еще и транспорные функции, т.е. входит в класс трансфераз.
К классу оксидоредуктаз относят цитохромы (от греч. cito — клетка, hro- mos — цвет). Из названия ясно, что это окрашенные соединения. По своей при-
Рис. 6.23. Перенос атомов Н липосвой кислотой
роде — это сложные белки хромопротеины. Небелковая часть цитохромов представляет собой гем (рис. 6.24), подобный гему в гемоглобине. Основу гема составляет порфиновое кольцо, которое образуется из четырех пиррольных циклов и метановых групп. В центре порфинового кольца находится атом железа. Поэтому цитохромы и подобные им структуры часто называют железопорфиринами.
Рис. 6.24. Гем и его структурные компоненты
В зависимости от строения гема все цитохромы делят на классы: А, В, С и D. В каждом классе выделяют индивидуальные цитохромы, которые различаются по составу белковой части. Индивидуальные цитохромы обозначают соответствующими латинскими буквами с индексом: av ft, и т.д. Другой способ обозначения индивидуальных цитохромов — указание в индексе характерной длины волны, при которой происходит поглощение в видимой области спектра.
Катион железа в цитохромах участвует в транспорте электронов и обратимо превращается из трехвалентного в двухвалентный (рис. 6.25).
Важной особенностью цитохромов является их способность агрегировать и образовывать цитохромную систему. Принимая электроны от субстрата или от других ферментов, цитохромы передают их по цепочке друг другу, осуществляя окислительно-восстановительные превращения (см. параграф 9.3).
Каталаза и пероксидаза также содержат гемовое железо (гемопротеины, железопорфирины), которое участвует в переносе электронов. Оба фермен-
Рис. 6.25. Схема участия цитохромов в окислительно-восстановительных процессах
та являются компонентами антиоксидантном системы организма и разлагают ядовитый пероксид водорода с образованием нескольких нетоксичных продуктов:
Оба фермента обнаружены в молоке. Содержание каталазы в молоке зависит от ряда зоотехнических факторов: рациона кормления, периода лактации, но, главным образом, от наличия воспалительных процессов в вымени, которые сопровождаются повышенным содержанием соматических клеток в молоке, что установлено по прямо пропорциональной зависимости между этими показателями. Поэтому высокое содержание каталазы в молоке обычно связано с той или иной формой мастита.
Каталаза молока наиболее активна в нейтральной среде (pH 7,0) при 38°С. При пастеризации каталаза разрушается, а если обнаруживается в пастеризованном молоке, то это каталаза бактериального происхождения.
Пероксидазу молока называют лактопероксидаза. Она связана с а-лакт- альбумином сывороточных белков молока и может составлять до 1% общего количества всех сывороточных белков, что намного больше, чем содержание других ферментов. Особенно высоким содержанием лактопероксидазы отличаются молозиво и маститное молоко. Это связано с тем, что данный фермент действует как компонент лактопероксидазной (антибактериальной) системы, уничтожающей патогенные микроорганизмы.
Наибольшую активность лактопероксидаза проявляет при pH 6,8. Она выщенляет из пероксида атомарный кислород и переносит его на легко окисляемые агенты (ароматические амины и кислоты, фенолы, >ТО2-ионы и тиоцианат). Многие из катализируемых лактоиероксидазой реакций сопровождаются изменением цвета, что используют в производственной практике как индикатор на наличие лактопероксидазы. Нагревание до 85°С в течение 10 с гарантированно ее инактивирует, поэтому тест на лактопе- роксидазу используют для контроля режимов температурной обработки молока и сливок.
К классу оксидоредуктаз относится ксаптипоксидаза, обнаруживаемая в молоке. Ее часто называют ферментом Шардингера, по фамилии первооткрывателя. Субстратами ксантиноксидазы являются ксантин, гипоксантин и альдегиды, а также нитраты (NO:3), которые восстанавливаются до нитритов (N02). Продуктами окисления ксантиноксидазы являются кислоты и супероксидные радикалы, поэтому ее относят к прооксидантам.
В организме человека и животных ксантиноксидаза завершает обмен пуриновых оснований образованием мочевой кислоты (рис. 6.26).
Этот фермент имеет олигомерную структуру, состоит из двух субъединиц. В активном центре каждой субъединицы находится кофермент ФАД. Кроме этого с молекулой ксантиноксидазы связаны четыре атома железа и один атом молибдена. Считается, что весь Мо молока входит в состав ксантиноксидазы, и дефицит этого минерала в рационе животных приводит к снижению активности ксантиноксидазы.
Рис. 6.26. Участие ксантиноксидазы в окислении ксантина
В молоке преимущественное количество ксантиноксидазы связано с белками оболочек жировых шариков, поэтому в первую очередь она усиливает процессы окислительной порчи молочного жира. Однако, пока ксантинок- сидаза связана с оболочками молочного жира, она малоактивна. Как только ксантиноксидаза становится свободной, ативность ее повышается. Это может произойти во многих технологических процессах, затрагивающих целостность оболочек жировых шариков молока.
Например, гомогенизация — процесс, требующий намеренного разрушения фосфолипидных оболочек шариков жира. Обычное резервирование молока при 4°С в течение 24 ч сопровождается кристаллизацией молочного жира, а следовательно, и частичным повреждением его оболочек. При нагреве до 70°С в течение 5 мин из таких жировых шариков происходит вытапливание некоторого количества свободного жира. Эти и другие операции, связанные с получением, хранением, транспортировкой и переработкой молока могут способствовать освобождению ксантиноксидазы и ее непосредственному контакту с молочным жиром. Поскольку этот фермент проявляет прооксидантиые свойства, он провоцирует увеличение окислительных процессов в продукте. По данным А. Тенела, молоко с признаками окислительной порчи содержит в 10 раз больше ксантиноксидазы, чем нормальное молоко.
Ферментом антиоксидантной защитной системы организма является супероксиддисмутаза (СОД), нейтрализующая ионы супероксида (О^), возникающие в различных окислительно-восстановительных процессах, в частности, при действии ксантиноксидазы. СОД разлагает их с образованием пероксида и молекулярного кислорода:
Хорошо изучена СОД крови крупного рогатого скота. Это димер, содержащий атомы Си и Zn, свободные SH-группы и одну S—S-связь. Предполагают, что СОД молока имеет идентичное строение. Установлено, что содержание СОД в молоке пропорционально содержанию ксантиноксидазы. Это свидетельствует о том, что СОД синтезируется для компенсации негативного действия ксантиноксидазы.
В молоке СОД сохраняет активность после нагревания до 71°С в течение 30 мин [261.
К классу оксидоредуктаз относятся гидроксилазы, которые катализируют присоединение только одного атома кислорода из его молекулы. Второй атом при этом идет на окисление восстановленных форм НАДН и НАДФН. Гидроксилазы очень активны в надпочечниках млекопитающих. С участием этих ферментов идут многие стадии синтеза стероидных гормонов (см. практический пример 1 в гл. 8).
источник
Общая характеристика класса оксидоредуктаз. Коферменты и простеические группы оксидоредуктаз. Привести конкретные примеры метаболических реакций с участием дегидрогеназ и оксидаз.
Оксидоредуктазы — Ферменты этого класса катализируют окислительно-восстановительные реакции, лежащие в основе биологического окисления. Класс насчитывает 22 подкласса. Коферментами этого класса являются НАД,НАДФ, ФАД, ФМН, убихинон, глутатион, липоевая кислота.
Примером подклассов могут служить ферменты, действующие на СН-ОН-группу доноров, на СH-СН-группу доноров, на СН-NН2-группу доноров, на гемсодержащие доноры.
Если рассматривать все подклассы, то в них выделяются группы ферментов, действующие на:
1.1. CH-OH группу доноров;
1.2. альдегидную или кетоновую группу доноров;
1.3. CH-СH группу доноров;
1.4. CH-NH2 группу доноров;
1.5. CH-NН группу доноров;
1.6. НАДH или НАДФН в качестве доноров;
1.8. содержащие серу группы доноров;
1.9. гем-содержащие доноры;
1.10. дифенолы в качестве доноров;
1.11. пероксид водорода в качестве акцептора;
1.11. водород в качестве донора;
1.13. один донор с включением молекулярного кислорода;
1.14. два донора с включением молекулярного кислорода;
1.15. супероксидные радикалы в качестве акцептора;
1.17. СН2 группу доноров;
1.18. ферредоксин в качестве донора;
1.19. флаводоксин в качестве донора;
1.20. фосфор или мышьяк в качестве донора;
1.21. на вещества Х-Н и Y-Н с образованием X-Y-связи;
1.22. галоген в качестве донора;
1.97. другие оксидоредуктазы.
На подподклассы деление производится в зависимости от акцептора – НАД+ или НАДФ+ (1.1.1., 1.2.1., 1.3.1., 1.4.1.), дисульфиды (1.2.4.), кислород (1.3.3.). Например, каталаза (КФ 1.11.1.6), пероксидаза (КФ 1.11.1.7).
Наиболее распространены следующие рабочие названияоксидоредуктаз:
1. Дегидрогеназы – оксидоредуктазы, катализирующие дегидрирование субстрата с использованием в качестве акцептора водорода любых молекул, кроме кислорода.
2. Если перенос водорода от молекулы донора трудно доказуем, то такие оксидоредуктазы называют редуктазами.
3. Оксидазы – оксидоредуктазы, катализирующие окисление субстратов с молекулярным кислородом в качестве акцептора электронов без включения кислорода в молекулу субстрата.
4. Монооксигеназы – оксидоредуктазы, катализирующие внедрение одного атома кислорода в молекулу субстрата с молекулярным кислородом в качестве донора кислорода.
5. Диоксигеназы – оксидоредуктазы, катализирующие внедрение 2 атомов кислорода в молекулу субстрата с молекулярным кислородом в качестве донора кислорода.
6. Пероксидазы – оксидоредуктазы, катализирующие реакции с пероксидом водорода в качестве акцептора электронов.
Характеристика фермента
| Систематическое название | Сукцинат:ФАД-оксидоредуктаза |
| Рабочее название | Сукцинатдегидрогеназа |
| Класс | 1. Оксидоредуктазы |
| Подкласс | 1.3. Действующие на СН-СН-группу доноров |
| Подподкласс | 1.3.99. с ФАД + в качестве акцептора |
| Кофакторы | Флавинадениндинуклеотид |
Характеристика фермента
| Систематическое название | Фенилаланин.Тетрагидробиоптерин:кислород-оксидоредуктаза |
| Рабочее название | Фенилаланин-4-монооксигеназа Фенилаланин-гидроксилаза |
| Класс | 1. Оксидоредуктазы |
| Кофакторы | Тетрагидробиоптерин. Железо. |
Общая характеристика класса трансфераз. Коферметны трансфераз. Привести конкретные примеры метаболических реакций с участием трансфераз. Диагностическое значение определения аминотрансфераз в сыворотке крови.
Трансферазы катализируют реакции переноса различных групп от одного субстрата (донор) к другому (акцептор), участвуют в реакциях взаимопревращения различных веществ, обезвреживания природных и чужеродных соединений. Коферментами являются пиридоксальфосфат, коэнзим А, тетрагидрофолиевая кислота, метилкобаламин. Класс подразделяется на 9 подклассов в зависимости от строения переносимых групп.
Примером подклассов являются ферменты, переносящие одноуглеродные фрагменты, альдегидные или кетоостатки, ацильные остатки, азотсодержащие группы, фосфорсодержащие группы.
Если рассматривать все подклассы, то в них выделяются группы ферментов в зависимости от состава переносимой группы
2.1. переносящие одноуглеродные фрагменты;
2.2. переносящие альдегидные и кетогруппы;
2.3. переносящие ацильные группы;
2.4. переносящие гликозильные группы;
2.5. переносящие неметильные алкильные и арильные группы;
2.6. переносящие азотсодержащие группы;
2.7. переносящие фосфорсодержащие группы.
2.8. переносящие сульфосодержащие группы;
2.9. переносящие селенсодержащие группы.
Часто встречается рабочее название трансфераз – киназы. Это трансферазы, катализирующие перенос фосфата от АТФ на субстрат (моносахариды, белки и др), т.е. фосфотрансферазы.
Систематическое название образуется:
Донор группы : акцептор группы – переносимая группа трансфераза.
Характеристика фермента
| Систематическое название | АТФ:D-гексоза-6-фосфотрансфераза |
| Рабочее название | Гексокиназа |
| Класс | 2. Трансферазы |
| Кофакторы | Магний |
Характеристика фермента
| Систематическое название | L-Аспартат:2-оксоглутарат-аминотрансфераза |
| Рабочее название | Аспартатаминотрансфераза |
| Класс | 2. Трансферазы |
| Кофактор | Пиридоксальфосфат |
Аминотрансферазы (трансаминазы) — ферменты, катализирующие межмолекулярный перенос аминогруппы от соответствующих аминокислот на a‑кетокислоты (2‑оксокислоты) с образованием новых кето- и аминокислот без образования свободного аммиака, в качестве кофермента используется витамин В6 (пиридоксин). Эти ферменты играют центральную роль в обмене белков, осуществляя окислительное дезаминирование аминокислот опосредованно через глутаминовую кислоту. Образующаяся глутаминовая кислота дезаминируется глутаматдегидрогеназой с освобождением свободного аммиака и 2‑оксоглутаровой кислоты.
В организме наибольшее значение имеют две аминотрансферазы: аспартатаминотрансфераза (АСТ или АсАТ) и аланинаминотрансфераза (АЛТ или АлАТ). В клинической практике чаще всего определяют именно активность этих двух ферментов. Реакции, катализируемые этими ферментами:
2-Оксоглутарат + Аспартат ↔ Глутамат + Оксалоацетат
2-Оксоглутарат + Аланин ↔ Глутамат + Пируват
Наибольшая активность АСТ обнаружена в миокарде, затем в порядке убывания в печени, скелетных мышцах, головном мозге, почках. Активность фермента в миокарде в 10000 раз выше, чем в сыворотке крови. Активность АЛТ максимальна в печени, среди других органов убывает в последовательности: поджелудочная железа, сердце, скелетные мышцы, селезенка, легкие. Избирательная тканевая локализация позволяет считать трансаминазы маркерными ферментами: АСТ для миокарда, АЛТ для печени. Соотношение активности аминотрансфераз позволяет судить о глубине повреждения клеток: АЛТ преимущественно локализована в цитоплазме, АСТ — в цитоплазме и в митохондриях.
Определение активности АСТ и АЛТ является чувствительным тестом для диагностики инфаркта миокарда, который не выявляется на ЭКГ, активность АСТ возрастает через 4‑6 часов от начала ангинального приступа, спустя 24‑36 часов достигает максимума и нормализуется на 3‑7 день. Вторичное повышение свидетельствует о повторном инфаркте. Особенно важное значение имеет определение активности аминотрансфераз для диагностики заболеваний печени. Некроз или повреждение печеночных клеток любой этиологии (острый и обострения хронического гепатита, холестатическая и обтурационная желтуха, лекарственно-индуцированное поражение) сопровождаются повышением активности обоих ферментов, преимущественно АЛТ, коэффициент де Ритиса = АСТ/АЛТ
Дата добавления: 2018-08-06 ; просмотров: 663 ; ЗАКАЗАТЬ РАБОТУ
источник